Bioorganinės chemijos dalykas. Bioorganinė chemija (BOC), jos svarba medicinoje
“ … Buvo tiek daug nuostabių nutikimų
Kad dabar jai nieko neatrodė įmanoma ”
L. Carroll „Alisa stebuklų šalyje“
Bioorganinė chemija išsivystė ant dviejų mokslų: chemijos ir biologijos ribos. Šiuo metu prie jų prisijungia medicina ir farmakologija. Visi keturi šie mokslai naudoja šiuolaikinius fizinių tyrimų, matematinės analizės ir kompiuterinio modeliavimo metodus.
1807 m Y. Aš. Berzelius pasiūlė, kad tokios medžiagos kaip alyvuogių aliejus arba cukrus, kurie yra įprasti gamtoje, turėtų būti vadinami ekologiškas.
Tuo metu jau buvo žinoma daug natūralių junginių, kurie vėliau pradėti apibrėžti kaip angliavandeniai, baltymai, lipidai, alkaloidai.
1812 metais rusų chemikas K.S. Kirchhoffas krakmolą, kaitinant jį rūgštimi, pavertė cukrumi, vėliau vadinamu gliukoze.
1820 metais prancūzų chemikas A. Brakonno perdirbdamas baltymą želatina, jis gavo glicino medžiagą, priklausančią junginių klasei, kuri vėliau Berzelius pavadintas amino rūgštys.
Organinės chemijos gimimo data galima laikyti 1828 m F. Velerakuris pirmą kartą sintetino natūralios kilmės medžiagą – karbamidas iš neorganinio amonio cianato junginio.
1825 metais fizikas Faradėjus atskyrė benzolą nuo dujų, kurios buvo naudojamos Londono miestui apšviesti. Benzeno buvimas gali paaiškinti dūminę Londono žibintų liepsną.
1842 m. N.N. Zininas pagaminta sintetika anilinas,
1845 metais A.V. F. Wöhlerio mokinys Kolbe iš pradinių elementų (anglies, vandenilio, deguonies) sintetino acto rūgštį - neabejotinai natūralų organinį junginį.
1854 m P. M. Berthelotpašildytą gliceriną su stearino rūgštimi ir gautą tristeariną, kuris pasirodė tapatus (identiškas) natūraliam junginiui, izoliuotam iš riebalų. Toliau P.M. Berthelot paėmė kitas rūgštis, kurios nebuvo izoliuotos iš natūralių riebalų, ir gavo junginius, labai panašius į natūralius riebalus. Tuo prancūzų chemikas įrodė, kad įmanoma gauti ne tik natūralių junginių analogus, bet ir kurti naujus, panašius ir tuo pačiu skirtingus nuo natūralių.
Daugelis svarbiausių organinės chemijos pasiekimų XIX a. Antrojoje pusėje yra susiję su natūralių medžiagų sinteze ir tyrimais.
1861 m. Vokiečių chemikas Friedrichas Augustas Kekule von Stradonitzas (mokslinėje literatūroje visada vadinamas Kekulé) išleido vadovėlį, kuriame organinę chemiją jis apibrėžė kaip anglies chemiją.
1861-1864 m. Rusijos chemikas A.M. Butlerovas sukūrė vieningą struktūros teoriją organiniai junginiai, kuris leido visus turimus pasiekimus perkelti į vieną mokslinį pagrindą ir atvėrė kelią organinės chemijos mokslo plėtrai.
Tuo pačiu laikotarpiu D. I. Mendelejevas. visame pasaulyje žinomas kaip mokslininkas, atradęs ir suformulavęs periodinį elementų savybių pokyčių dėsnį, išleidęs vadovėlį „Organinė chemija“. Mūsų žinioje yra jo antrasis leidimas. (Pataisyta ir papildyta, Asociacijos „Visuomenės nauda“ leidinys, Sankt Peterburgas, 1863, 535 s)
Savo knygoje didysis mokslininkas aiškiai apibrėžė santykį tarp organinių junginių ir gyvybiškai svarbių procesų: „Daugelį tų procesų ir medžiagų, kurias gamina organizmai, galime dauginti dirbtinai, už organizmo ribų. Taigi baltyminės medžiagos, sunaikinamos gyvūnuose veikiant kraujyje įsisavinamam deguoniui, virsta amoniako druskomis, karbamidu, gleivių cukrumi, benzenkarboksirūgštimi ir kitomis medžiagomis, paprastai išsiskiriančiomis su šlapimu. , bet atliekama pagal bendruosius gamtos dėsnius". Tomis dienomis bioorganinė chemija ir biochemija dar nebuvo susiformavę
nepriklausomos kryptys, iš pradžių jos buvo vieningos fiziologinė chemijabet palaipsniui jie, remiantis visais pasiekimais, išaugo į du nepriklausomus mokslus.
Bioorganinės chemijos mokslo studijos organinių medžiagų struktūros ir jų biologinių funkcijų ryšys, daugiausia naudojant organinės, analitinės, fizinės chemijos, taip pat matematikos ir fizikos metodus
Pagrindinis šio dalyko skiriamasis bruožas yra medžiagų biologinio aktyvumo tyrimas, susijęs su jų cheminės struktūros analize.
Bioorganinės chemijos tyrimo objektai: biologiškai svarbūs natūralūs biopolimerai - baltymai, nukleorūgštys, lipidai, mažos molekulinės masės medžiagos - vitaminai, hormonai, signalinės molekulės, metabolitai - medžiagos, dalyvaujančios energijos ir plastikos apykaitoje, sintetiniai narkotikai.
Pagrindinės bioorganinės chemijos užduotys apima:
1. Izoliacijos, natūralių junginių gryninimo metodų kūrimas, medicininių metodų naudojimas vertinant vaisto (pavyzdžiui, hormono pagal jo aktyvumo laipsnį) kokybę;
2. Natūralaus junginio struktūros nustatymas. Taikomi visi chemijos metodai: molekulinės masės nustatymas, hidrolizė, funkcinių grupių analizė, optinių tyrimų metodai;
3. Natūralių junginių sintezės metodų kūrimas;
4. Biologinio veikimo priklausomybės nuo struktūros tyrimas;
5. Biologinio aktyvumo pobūdžio, sąveikos su įvairiomis ląstelių struktūromis ar jos komponentais molekulinių mechanizmų išaiškinimas.
Bioorganinės chemijos raida dešimtmečiais siejama su Rusijos mokslininkų vardais:D. I. Mendelejeva, A. M. Butlerova, N. N. Zinin, N. D. Zelinsky, A. N. Belozersky, N. A. Preobrazhensky, M. M. Shemyakin, Yu.A. Ovčinnikovas.
Bioorganinės chemijos steigėjai užsienyje yra mokslininkai, padarę daug svarbių atradimų: antrinės baltymo struktūros struktūrą (L. Pauling), visišką chlorofilo, vitamino B 12 (R. Woodward) sintezę, fermentų naudojimą sintezuojant sudėtingas organines medžiagas. įskaitant geną (G. Koranas) ir kitus
Uraluose Jekaterinburge bioorganinės chemijos srityje nuo 1928 iki 1980 m. dirbo UPI akademiko Organinės chemijos katedros vedėju I.Ya.Putovsky, žinomas kaip vienas iš mūsų šalies mokslinių vaistų paieškos ir sintezės krypties įkūrėjų ir daugelio vaistų (sulfonamidai, priešnavikiniai, antiradiaciniai, prieštuberkulioziniai) autoriai .. Jo tyrimus tęsia dirbantys studentai. vadovaujant akademikams O. N. Chupakhinui, V. N. Charushinas USTU-UPI ir Organinės sintezės institute, pavadintame IR AŠ. Rusijos mokslų akademijos Postovskis.
Bioorganinė chemija yra glaudžiai susijusi su medicinos užduotimis, ji reikalinga biochemijos, farmakologijos, patofiziologijos ir higienos tyrimams ir supratimui. Visa mokslinė bioorganinės chemijos kalba, priimtas žymėjimas ir naudojami metodai nesiskiria nuo organinės chemijos, kurios mokėtės mokykloje
Bioorganinės chemijos dalykas.Organinių medžiagų struktūra ir izomerija
jungtys.
Cheminis ryšys ir sąveika
organiniuose junginiuose esantys atomai.
Cheminių reakcijų tipai.
Poli- ir heterofunkciniai
jungtys.
Pagrindinis vadovėlis - Tyukavkina N.A., Baukov Yu.I.
Bioorganinė chemija.
Paskaitų ir vadovo „Bioorganinė chemija
klausimai ir atsakymai “žr. TSU svetainėje http://tgumed.ru
skirtukas „Pagalba studentams“, skyrius „Paskaitos įjungtos
mokymo programos disciplinos “. Ir, žinoma, VK
Bioorganinė chemija tiria medžiagų, dalyvaujančių gyvenimo procesuose, struktūrą ir savybes, susijusias su jų biologinėmis žiniomis
Bioorganinė chemija tiria medžiagų struktūrą ir savybesdalyvavimas gyvenimo procesuose, susijęs su
žinios apie jų biologines funkcijas.
Pagrindiniai tyrimo objektai yra biologiniai
polimerai (biopolimerai) ir bioreguliatoriai.
Biopolimerai
–
didelė molekulinė masė
natūralus
junginiai, kurie yra struktūrinis visų gyvų pagrindas
organizmus ir vaidina svarbų vaidmenį procesuose
gyvenimo veikla. Biopolimerai apima peptidus ir
baltymai, polisacharidai (angliavandeniai), nukleorūgštys. AT
šiai grupei priklauso ir lipidai, kurie patys savaime nėra
yra didelės molekulinės masės junginiai, tačiau
kūnas paprastai yra susijęs su kitais biopolimerais.
Bioreguliatoriai yra chemiškai junginiai
reguliuoti medžiagų apykaitą. Tai apima vitaminus,
hormonai, daugelis sintetinių biologiškai aktyvių
junginiai, įskaitant vaistines medžiagas.
Organizme vykstančių cheminių reakcijų rinkinys vadinamas medžiagų apykaita arba metabolizmu. Medžiagos, susidariusios ląstelėse, mk
Cheminių organizmo reakcijų rinkinys,vadinamas metabolizmu arba metabolizmu. Medžiagos,
susidaro augalų ir gyvūnų ląstelėse, audiniuose ir organuose
metabolizmo procese vadinami metabolitais.
Metabolizmas apima dvi sritis - katabolizmą ir
anabolizmas.
Katabolizmas reiškia įeinančių medžiagų skaidymo reakcijas
į organizmą su maistu. Paprastai juos lydi organinių junginių oksidacija ir jie išsiskiria
energijos.
Anabolizmas yra sudėtingų molekulių sintezė iš
paprastesnis, dėl kurio susidaro ir atsinaujina gyvo organizmo struktūriniai elementai.
Metaboliniai procesai vyksta dalyvaujant fermentams,
tie. specifiniai baltymai, esantys ląstelėse
organizmą ir atlieka biocheminių katalizatorių vaidmenį
procesai (biokatalizatoriai).
Metabolizmas
katabolizmasanabolizmas
Biopolimerų skaidymas
su akcentu
energijos
Biopolimerų sintezė
su absorbcija
energijos
Glicerinas ir
riebalų rūgštis
Pagrindinės organinių junginių struktūros teorijos nuostatos A.M. Butlerova
1. Atomai molekulėje yra tam tikroje vietojesekos pagal jų valentingumą.
Organinio anglies atomo valentingumas
ryšiai yra keturi.
2. Medžiagų savybės priklauso ne tik nuo ko
atomai ir kiek jų yra
molekules, bet ir jų eilės tvarka
tarpusavyje susiję.
3. Atomai arba jų grupės
molekulės, viena kitai daro įtaką, iš kurios
cheminis aktyvumas ir reakcija
molekulių gebėjimas.
4. Medžiagų savybių tyrimas leidžia nustatyti jų savybes
cheminė struktūra.
G o m o l o g ir ch e c i y r i d
Homologiškaseilutė
Nemažai struktūriškai panašių junginių
panašių cheminių savybių, kurių individas
serijos nariai skiriasi vienas nuo kito tik suma
grupės -CH2- vadinamos homologinėmis eilėmis, o grupė
CH2 - homologinis skirtumas.
Bet kurios homologiškos serijos nariai turi didžiulį įspūdį
dauguma reakcijų vyksta vienodai (išimtis
sudaro tik pirmuosius serijos narius). Todėl žinodamas
tik vieno serijos nario chemines reakcijas galima su
labai tikėtina, kad tvirtins tą patį
transformacijos tipas taip pat vyksta su likusiais nariais
homologinė serija.
Bet kuriai homologinei serijai galima gauti
bendroji formulė, atspindinti santykį tarp atomų
anglis ir vandenilis šios serijos nariuose; tokia formulė
vadinama bendra homologinių eilučių formulė.
Organinių junginių klasifikavimas pagal anglies skeleto struktūrą
Organinių junginių klasifikavimas pagal funkcines grupes
Funkcinė grupėKlasė
Pavyzdys
halogeno atomai (F, Cl, Br, I) halogeno dariniai СН3СН2Cl (chloretanas)
hidroksilas (–OH)
alkoholiai (fenoliai)
CH3CH2OH (etanolis)
tiolis arba merkapto- (- tiolai (merkaptanai) CH3CH2SH (etanolio)
SН)
eterinis (–O–)
eteriai
CH3CH2-O-CH2CH3
(dietil
eteris)
esteris
karboksil-C JT
esteriai
CH3CH2COOCH3 (metilacetatas)
karboksirūgštys CH3COOH (acto rūgštis)
amidas –C ОNН2
amidai
karbonilas (–C \u003d O)
sulfo- (-SO3H)
amino (–NH2)
aldehidai ir
ketonai
sulfoninės rūgštys
aminai
nitro- (–NO2)
nitro junginiai
rūgštys
CH3CONH2 (acetamidas)
CH3CHO (etanalas)
CH3COCH3 (propanonas)
CH3SO3H (metansulfono rūgštis)
CH3CH2NH2
(etilaminas,
pirminis aminas)
CH3NHCH3
(dimetilaminas,
antrinis aminas)
CH3CH2NO2 (nitroetanas)
Organinių junginių nomenklatūra
Organinių junginių izomerija
Jei turi dvi ar daugiau atskirų medžiagųta pati kiekybinė sudėtis (molekulinė formulė),
bet skiriasi viena nuo kitos rišimosi seka
atomai ir (ar) jų išsidėstymas erdvėje, tada apskritai
jie vadinami izomerais.
Kadangi šių junginių struktūra yra skirtinga, tada
cheminis arba fizinės savybės izomerai
skiriasi.
Izomerijos tipai: struktūriniai (struktūriniai izomerai) ir
stereoizomerizmas (erdvinis).
Struktūrinė izomerija gali būti trijų tipų:
- anglies skeleto izomerija (grandinės izomerai),
- padėties izomerai (daugybė jungčių arba funkciniai
grupės),
- funkcinės grupės (tarpklasės) izomerai.
Stereoizomerizmas yra suskirstytas
konfigūracija
ant
konformacinis
ir
Tai tokia geometrinė izomerija
Lėktuvo poliarizuota šviesa
Optinio aktyvumo požymiai:- asimetrinio anglies atomo buvimas;
- molekulės simetrijos elementų nebuvimas
Adrenalino enantiomerai
baltymas
Anijoninis
Butas
Centras
paviršius
neužimtas
Butas
Anijoninis
paviršius
Centras
užsiėmes
(+) - adrenalinas
(-) - adrenalinas
Nebaigtas
atitikimas
žemas
veikla
baigtas
atitikimas
aukštas
veikla
Biologinis enantiomerų aktyvumas
asparaginasDARVONAS
analgetikas
NOVRADAS
vaistas nuo kosulio
veidrodis
L-asparaginas
D-asparaginas
(iš šparagų)
(iš žirnių)
kartus skonis
saldaus skonio
enantiomerai
Talidomido aukos
Organinių junginių rūgštingumas ir baziškumas
Bronzinės rūgštys (protoninės rūgštys) -neutralios molekulės ar jonai, galintys
paaukoti protoną (protonų donorai).
Tipiškos Bronstedo rūgštys yra karboksirūgštys
rūgštis. Silpnesnės rūgštinės savybės turi
fenolių ir alkoholių hidroksilo grupės, taip pat tio-,
amino ir imino grupės.
Bronzinės bazės yra neutralios molekulės arba
jonai, galintys prijungti protoną (akceptoriai
protonai).
Tipiškos Bronsted bazės yra aminai.
Amfolitai - junginiai, esantys molekulėse
kurios yra ir rūgščios, ir
pagrindinės grupės.
Brønstedo rūgšties ir bazės rūšys
Pagrindiniai novokaino molekulės centrai
Pagrindinių savybių naudojimas vandenyje tirpių vaistų formoms gauti
Pagrindinissavybės
vaistinis
narkotikai
yra naudojami jų vandenyje tirpioms formoms gauti.
Sąveikaujant su rūgštimis, junginiai susidaro su
joninės jungtys - druskos, gerai tirpstančios vandenyje.
Taigi, novokainas injekcijoms
naudojamas hidrochlorido pavidalu.
stipriausias pagrindinis centras,
prisijungė protonas
Rūgštinės medžiagų savybės ir jų patekimas į organizmą
lipidaimembrana
Skrandžio pH 1
UNSD
lipidai
membrana
kraujo plazma
pH 7,4
UNSD
OCOSN3
Skrandžio pH 1
+
OCOSN3
NH3
SOOOOSN3
SOO-
NH2
NH2
OCOSN3
Žarnyno pH 7–8
kraujo plazma
pH 7,4
Žarnyno pH 7–8
Rūgštiniai vaistai geriau absorbuojami iš skrandžio (pH 1-3),
ir absorbuojama tik vaistai ar ksenobiotikai
jiems patekus iš skrandžio į žarnyną (pH 7–8). Per
vieną valandą nuo žiurkių skrandžio absorbuojama beveik 60% acetilsalicilo
rūgšties ir tik 6% anilino nuo pavartotos dozės. Žiurkių žarnyne
jau absorbavo 56% suvartotos anilino dozės. Toks silpnas pamatas
kaip kofeinas (pKBH + 0,8), tuo pačiu metu absorbuojamas daug didesniame
laipsnio (36 proc.), nes net labai rūgščioje skrandžio aplinkoje kofeinas
yra daugiausia nejonizuotos būsenos.
Organinės chemijos reakcijų tipai
Organinės reakcijos skirstomos pagalšie ženklai:
1. Pagal reagentų elektroninį pobūdį.
2. Dalelių skaičiaus pokyčiu reakcijos metu.
3. Privačiais ženklais.
4. Elementarių mechanizmais
reakcijų stadijos.
Atsižvelgiant į reagentų elektroninį pobūdį, išskiriamos reakcijos: nukleofilinės, elektrofilinės ir laisvieji radikalai
Laisvieji radikalai yra elektriniu požiūriu neutralios dalelės,turintis nesuporuotą elektroną, pavyzdžiui: Cl, NO2.
Alkanams būdingos laisvųjų radikalų reakcijos.
Elektrofiliniai reagentai yra katijonai arba molekulės
kurie patys arba dalyvaujant katalizatoriui
turėti didesnį afinitetą elektroninei porai arba
neigiamai įkrautų molekulių centrų. Jie apima
katijonai H +, Cl +, + NO2, + SO3H, R + ir molekulės su laisvaisiais
orbitos AlCl3, ZnCl2 ir kt.
Elektrofilinės reakcijos būdingos alkenams, alkinams,
aromatiniai junginiai (dvigubo ryšio junginys,
protonų pakeitimas).
Nukleofiliniai reagentai yra anijonai ar molekulės, kurios
turintys padidinto elektronų tankio centrus. Jiems
apima anijonus ir molekules, tokias kaip
HO-, RO-, Cl-, Br-, RCOO-, CN-, R-, NH3, C2H5OH ir kt. Pakeitimais
dalelių skaičius eigoje
reakcijos išskiria
pakaitinės reakcijos,
prisijungimas,
atsiskyrimas
(pašalinimas),
skilimas
Reakcijų klasifikavimas pagal konkrečias charakteristikas
Visada atsižvelgiama į reaktyvumą
tik reakcinio partnerio atžvilgiu.
Cheminės konversijos metu paprastai
paveikta ne visa molekulė, o tik dalis jos -
reakcijos centras.
Organiniame junginyje gali būti
keli nelygios reakcijos centrai.
Reakcijos gali sukelti izomerinius produktus.
Reakcijos selektyvumas - kokybinis
būdinga reikšmė lengvatinė
reakcija vyksta viena kryptimi nuo
keli galimi.
Atskirti regioselektyvumą,
chemoselektyvumas, reakcijos stereoselektyvumas.
Reakcijų selektyvumas organinėje chemijoje
Regioselektyvumas - pageidaujama reakcijos eigavienas iš kelių molekulės reakcijos centrų.
CH3-CH2-CH3 + Br2
CH3-CHBr-CH3 + HBr
Antrasis izomeras, 1-brompropanas, praktiškai nesusidaro.
Chemijos selektyvumas - pageidaujama reakcijos eiga
viena iš susijusių funkcinių grupių.
Stereoselektyvumas yra pageidautinas reakcijos formavimas
vienas iš kelių galimų stereoizomerų. Polifunkciniuose junginiuose yra
kelios identiškos funkcinės grupės.
Heterofunkciniuose junginiuose yra
kelios skirtingos funkcinės grupės.
Heteropolifunkcinis
junginiuose yra kaip
skirtingas ir tas pats
funkcinės grupės.
Poli- ir heterofunkcinių junginių savybės
Kiekviena grupė yra poli- ir heterofunkcinėjunginiai gali vykti į tas pačias reakcijas kaip ir
monofunkcinė grupė
jungtys Specifinės poli- ir
heterofunkciniai junginiai
Ciklizacijos reakcijos
Chelatinių kompleksų susidarymas Polifunkciniai junginiai kaip priešnuodžiai
Toksiškas poveikis sunkieji metalai susideda iš
tiolio baltymų grupių prisijungimas. Dėl to
gyvybiškai svarbūs organizmo fermentai.
Priešnuodžių veikimo principas yra ilgalaikio susidarymas
kompleksai su sunkiųjų metalų jonais.
Gardinas "href \u003d" / text / category / grodno / "rel \u003d" bookmark "\u003e Gardino valstybinis medicinos universitetas", chemijos mokslų kandidatas, docentas;
Švietimo įstaigos „Gardino valstybinis medicinos universitetas“ Bendrosios ir bioorganinės chemijos katedros docentas, biologijos mokslų kandidatas, docentas
Recenzentai:
Švietimo įstaigos „Gomelio valstybinis medicinos universitetas“ Bendrosios ir bioorganinės chemijos katedra;
– galva Bioorganinės chemijos katedra Švietimo įstaiga "Baltarusijos valstybinis medicinos universitetas", medicinos mokslų kandidatas, docentas.
Švietimo įstaigos "Gardino valstybinis medicinos universitetas" Bendrosios ir bioorganinės chemijos katedra
(minutės nuo 01.01.01)
Švietimo įstaigos „Gardino valstybinis medicinos universitetas“ centrinė mokslinė ir metodinė taryba
(minutės nuo 01.01.01)
Baltarusijos Respublikos universitetų švietimo ir metodikos asociacijos medicinos medicinos psichologiniai reikalai
(minutės nuo 01.01.01)
Atsakingas už išleidimą:
Švietimo įstaigos „Gardino valstybinis medicinos universitetas“ pirmasis prorektorius, profesorius, medicinos mokslų daktaras
Aiškinamasis raštas
Akademinės disciplinos studijų aktualumas
„Bioorganinė chemija“
Bioorganinė chemija yra pagrindinė gamtos mokslo disciplina. Bioorganinė chemija kaip savarankiškas mokslas susiformavo XX a. Antrojoje pusėje organinės chemijos ir biochemijos sandūroje. Bioorganinės chemijos studijų aktualumas susijęs su praktinėmis problemomis, su kuriomis susiduria medicina ir žemės ūkis (vitaminų, hormonų, antibiotikų, augalų augimą stimuliuojančių medžiagų, gyvūnų ir vabzdžių elgesio reguliatorių ir kitų vaistų gavimas), kurių išspręsti neįmanoma nenaudojant teorinio ir praktinio bioorganinės chemijos potencialo.
Bioorganinė chemija nuolat praturtinama naujais natūralių junginių išskyrimo ir gryninimo metodais, natūralių junginių ir jų analogų sintezės metodais, žiniomis apie junginių struktūros ir biologinio aktyvumo ryšį ir kt.
Naujausi požiūriai į medicinos švietimą, susiję su reprodukcinio stiliaus įveikimu mokant, užtikrinant pažintinę ir tiriamąją studentų veiklą, taip pat atveria naujas perspektyvas realizuoti tiek individo, tiek komandos potencialą.
Disciplinos tikslas ir uždaviniai
Įvartis: cheminės kompetencijos lygio formavimas medicinos mokymo sistemoje, kuris užtikrina tolesnį biomedicinos ir klinikos disciplinų tyrimą.
Užduotys:
Studentų įsisavinimas teorinių organinių molekulių transformacijų, atsižvelgiant į jų struktūrą ir biologinį aktyvumą, pagrindų;
Susiformavimas: žinių apie molekulinius gyvenimo procesų pagrindus;
Organizuotų junginių, kurie veikia kaip vaistai, klasifikavimo, struktūros ir savybių įgūdžių lavinimas
Cheminio mąstymo logikos formavimas;
Gebėjimų naudotis kokybinės analizės metodais ugdymas
organiniai junginiai;
Cheminės žinios ir įgūdžiai, kurie yra cheminės kompetencijos pagrindas, padės formuoti absolvento profesinę kompetenciją.
Reikalavimai akademinės disciplinos ugdymui
Reikalavimai disciplinos „Bioorganinė chemija“ turinio įsisavinimo lygiui nustatomi pagal pirmojo etapo bendrojo profesinio ir specialiojo mokslo disciplinų aukštojo mokslo išsilavinimo standartą, kuris yra parengtas atsižvelgiant į kompetencijos požiūrio reikalavimus, kuriame nurodomas minimalus disciplinos turinys apibendrintų cheminių žinių ir įgūdžių, sudarančių bioorganinę kompetenciją, forma. universiteto absolventas:
a) apibendrintos žinios:
- suprasti dalyko kaip mokslo esmę ir jo santykį su kitomis disciplinomis;
Reikšmė suprasti medžiagų apykaitos procesus;
Organinių molekulių struktūros ir reaktyvumo vienovės samprata;
Pagrindiniai chemijos dėsniai, būtini gyvuose organizmuose vykstantiems procesams paaiškinti;
Pagrindinių organinių junginių klasių cheminės savybės ir biologinė reikšmė.
b) bendrieji įgūdžiai:
Numatyti reakcijos mechanizmą, remiantis žiniomis apie organinių molekulių struktūrą ir cheminių ryšių nutraukimo metodus;
Paaiškinkite reakcijų svarbą gyvenančių sistemų funkcionavimui;
Pasinaudokite gautomis žiniomis studijuodami biochemiją, farmakologiją ir kitas disciplinas.
Akademinės disciplinos struktūra ir turinys
Šioje programoje disciplinos „bioorganinė chemija“ turinio struktūrą sudaro įvadas į discipliną ir du skyriai, kurie apima bendruosius organinių molekulių reaktyvumo klausimus, taip pat hetero- ir polifunkcinių junginių, dalyvaujančių gyvybiškai svarbiuose procesuose, savybes. Kiekvienas skyrius yra suskirstytas į temas, išdėstytas tokia seka, kad būtų galima optimaliai išmokti ir įsisavinti programos medžiagą. Kiekvienai temai pateikiamos apibendrintos žinios ir įgūdžiai, kurie sudaro studentų bioorganinės kompetencijos esmę. Atsižvelgiant į kiekvienos temos turinį, apibrėžiami kompetencijos reikalavimai (apibendrintų žinių ir įgūdžių sistemos forma), kuriems formuoti ir diagnozuoti galima kurti testus.
Mokymo metodai
Pagrindiniai mokymo metodai, tinkamai atitinkantys šios disciplinos studijų tikslus, yra šie:
Paaiškinimas ir konsultacijos;
Laboratorinė pamoka;
Probleminio mokymosi elementai (mokinių edukacinis ir tiriamasis darbas);
Bioorganinės chemijos įvadas
Bioorganinė chemija kaip mokslas, tiriantis organinių medžiagų struktūrą ir jų transformaciją kartu su biologinėmis funkcijomis. Bioorganinės chemijos tyrimo objektai. Bioorganinės chemijos vaidmuo formuojant mokslinį pagrindą biologinių ir medicininių žinių suvokimui šiuolaikiniame molekuliniame lygmenyje.
Organinių junginių struktūros teorija ir jos raida dabartiniame etape. Organinių junginių izomerija kaip organinių junginių įvairovės pagrindas. Organinių junginių izomerizmo tipai.
Organinių junginių, kurie yra svarbūs biomedicininei analizei, išskyrimo ir tyrimo fizikiniai-cheminiai metodai.
Pagrindinės IUPAC organinių junginių nomenklatūros taisyklės: pakaitinė ir radikaliai funkcinė nomenklatūra.
Organinių molekulių erdvinė struktūra, jos ryšys su anglies atomo hibridizacijos tipu (sp3-, sp2- ir sp-hibridizacija). Stereocheminės formulės. Konfigūracija ir konformacija. Atviros grandinės konformacijos (užtemdytos, slopinamos, išlenktos). Konformacijų energinė charakteristika. Newmano projekcijos formulės. Tam tikrų grandinės dalių erdvinė konvergencija dėl konformacinės pusiausvyros ir kaip viena iš priežasčių, kodėl vyrauja penkių ir šešių narių žiedai. Ciklinių junginių (cikloheksano, tetrahidropirano) konformacija. Kėdės ir vonios konformacijų energijos charakteristikos Ašinės ir pusiaujo jungtys. Erdvinės struktūros santykis su biologiniu aktyvumu.
Kompetencijos reikalavimai:
Žinoti tyrimo objektus ir pagrindines bioorganinės chemijos užduotis,
· Gebėti klasifikuoti organinius junginius pagal anglies skeleto struktūrą ir funkcinių grupių pobūdį, naudoti sisteminės cheminės nomenklatūros taisykles.
· Žinoti pagrindinius organinių junginių izomerizmo tipus, mokėti pagal junginio struktūrinę formulę nustatyti galimus izomerų tipus.
· Žinoti įvairius anglies atomų orbitalių hibridizacijos tipus, atomo ryšių erdvinę orientaciją, jų tipą ir skaičių, atsižvelgiant į hibridizacijos tipą.
· Žinoti ciklinių (kėdžių, vonių) ir aciklinių (slopintų, iškreiptų, aptemtų konformacijų) molekulių konformacijų energetines charakteristikas, gebėti jas pavaizduoti Newmano projekcijos formulėmis.
· Žinoti įvairiose molekulėse kylančių įtempių tipus (sukimą, kampinį, van der Waalsą), jų poveikį konformacijos stabilumui ir visai molekulei.
1 skyrius. Organinių molekulių reaktyvumas dėl abipusės atomų įtakos, organinių reakcijų mechanizmai
1 tema. Konjuguotos sistemos, aromatiškumas, pakaitų elektroniniai efektai
Konjuguotos sistemos ir aromatiškumas. Konjugacija (p, p - ir p, p-konjugacija). Atviros grandinės konjuguotos sistemos: 1,3-dienai (butadienas, izoprenas), polienai (karotenoidai, vitaminas A). Sujungtos sistemos su uždara grandine. Aromatiškumas: aromatingumo kriterijai, Hückelio aromatingumo taisyklė. Benzenkarboksirūgščių (benzenas, naftalenas, fenantrenas) junginių aromatas. Konjugacijos energija. Karbo- ir heterociklinių aromatinių junginių termodinaminio stabilumo struktūra ir priežastys. Heterociklinių (pirolo, imidazolo, piridino, pirimidino, purino) junginių aromatas. Pirolio ir piridino azoto atomai, aromatinių sistemų perteklius ir trūkumas.
Abipusė atomų įtaka ir jos perdavimo organinėse molekulėse metodai. Elektronų delokalizacija kaip vienas iš veiksnių, didinančių molekulių ir jonų stabilumą, jo paplitimas biologiškai svarbiose molekulėse (porfinas, hemas, hemoglobinas ir kt.). Obligacijų poliarizacija. Elektroninis pakaitų (indukcinių ir mezomerinių) poveikis, kaip netolygaus elektronų tankio pasiskirstymo ir reakcijos centrų atsiradimo molekulėje priežastis. Indukcinis ir mezomerinis poveikis (teigiamas ir neigiamas), jų grafinis žymėjimas struktūrinėse organinių junginių formulėse. Elektronus dovanojantys ir pašalinantys elektronus pakaitalai.
Kompetencijos reikalavimai:
· Žinoti konjugacijos tipus ir mokėti nustatyti konjugacijos tipą pagal struktūrinę jungties formulę.
· Žinoti aromatingumo kriterijus, mokėti pagal struktūrinę formulę nustatyti priklausymą aromatiniams karbo- ir heterociklinių molekulių junginiams.
· Gebėti įvertinti elektroninį atomų indėlį kuriant vieną konjuguotą sistemą, žinoti elektroninę piridino ir pirolio azoto atomų struktūrą.
· Žinoti elektroninius pakaitalų padarinius, jų atsiradimo priežastis ir mokėti grafiškai pavaizduoti jų veikimą.
· Gebėti klasifikuoti pakaitalus kaip elektronų donorus arba elektronų akceptorius, atsižvelgiant į jų indukcinį ir mezomerinį poveikį.
· Gebėti numatyti pakaitų poveikį molekulių reaktyvumui.
2 tema. Angliavandenilių reaktyvumas. Radikalaus pakaitalo, elektrofilinio pridėjimo ir pakaitų reakcijos
Organinių junginių reaktyvumo, kaip cheminio jų biologinio funkcionavimo, bendrieji dėsniai. Cheminė reakcija kaip procesas. Sąvokos: substratas, reagentas, reakcijos centras, perėjimo būsena, reakcijos produktas, aktyvacijos energija, reakcijos greitis, mechanizmas.
Organinių reakcijų klasifikavimas pagal rezultatą (pridėjimas, pakeitimas, pašalinimas, redoksas) ir pagal mechanizmą - radikalus, joninius (elektrofilinius, nukleofilinius), nuoseklius. Reagento tipai: radikalūs, rūgštiniai, baziniai, elektrofiliniai, nukleofiliniai. Homolizinis ir heterolitinis kovalentinio ryšio suskaidymas organiniuose junginiuose ir susidariusiose dalelėse: laisvieji radikalai, karbokacijos ir karbanionai. Šių dalelių elektroninė ir erdvinė struktūra bei veiksniai, lemiantys jų santykinį stabilumą.
Angliavandenilių reaktyvumas. Radikalios pakaitų reakcijos: homolizinės reakcijos, susijusios su sp3-hibridizuoto anglies atomo CH jungtimis. Radikalų pakeitimo mechanizmas alkanų ir cikloalkanų halogeninimo reakcijos pavyzdžiu. Grandinės procesų samprata. Regioselektyvumo samprata.
Laisvųjų radikalų susidarymas: fotolizė, termolizė, redoksinės reakcijos.
Elektrofilinės pridėjimo reakcijos ( AE) nesočiųjų angliavandenilių serijoje: heterolitinės reakcijos, susijusios su p-ryšiu tarp sp2-hibridizuotų anglies atomų. Hidratacijos ir hidrohalogeninimo reakcijų mechanizmas. Rūgščių katalizė. Markovnikovo valdžia. Statinių ir dinaminių veiksnių įtaka elektrofilinių pridėjimo reakcijų regioselektyvumui. Elektrofilinio adeno su anglies angliavandeniliais ir mažų ciklų (ciklopropano, ciklobutano) reakcijų ypatybės.
Elektrofilinių pakaitų reakcijos ( SE): heterolitinės reakcijos, susijusios su aromatinės sistemos p-elektronų debesimi. Aromatinių junginių halogeninimo, nitrinimo, alkilinimo reakcijų mechanizmas: p - ir s- kompleksai. Katalizatoriaus (Lewiso rūgšties) vaidmuo formuojant elektrofilinę dalelę.
Aromatiniame žiede esančių pakaitų įtaka junginių reaktyvumui elektrofilinių pakaitų reakcijose. Pakaitų orientacinė įtaka (I ir II rūšies orientantai).
Kompetencijos reikalavimai:
· Žinoti substrato, reagento, reakcijos centro, reakcijos produkto, aktyvacijos energijos, reakcijos greičio, reakcijos mechanizmo sąvokas.
· Žinoti reakcijų klasifikaciją pagal įvairius kriterijus (pagal galutinį rezultatą, ryšių nutraukimo metodą, pagal mechanizmą) ir reagentų tipus (radikalius, elektrofilinius, nukleofilinius).
· Žinoti elektroninę ir erdvinę reagentų struktūrą bei veiksnius, lemiančius jų santykinį stabilumą, mokėti palyginti to paties tipo reagentų santykinį stabilumą.
· Žinoti laisvųjų radikalų susidarymo metodus ir radikalų pakaitalų (SR) reakcijų mechanizmą, pateikiant alkano ir cikloalakano halogeninimo reakcijų pavyzdžius.
· Gebėti nustatyti statistinę galimų produktų susidarymo tikimybę radikalių pakaitų reakcijose ir regioselektyvaus proceso srauto galimybę.
· Žinoti elektrofilinio papildymo (AE) reakcijų mechanizmą halogeninimo, hidrohalogeninimo ir alkenų hidratacijos reakcijose, mokėti kokybiškai įvertinti substratų reaktyvumą pagal elektroninių pakaitų poveikį.
· Žinoti Markovnikovo taisyklę ir mokėti nustatyti hidratacijos ir hidrohalogeninimo reakcijų regioselektyvumą remiantis statinių ir dinaminių veiksnių įtaka.
· Žinoti elektrofilinio prisijungimo prie konjuguotų dieninio angliavandenilių ir mažų ciklų (ciklopropano, ciklobutano) reakcijų ypatybes.
· Žinoti elektrofilinio pakaitalo (SE) reakcijų mechanizmą halogeninimo, nitrinimo, alkilinimo, aromatinių junginių acilinimo reakcijose.
· Gebėti, remiantis pakaitalų elektroniniu poveikiu, nustatyti jų įtaką aromatinio branduolio reaktyvumui ir orientuojančiam poveikiui.
3 tema. Organinių junginių rūgščių ir šarmų savybės
Organinių junginių rūgštingumas ir pagrindas: Bronstedo ir Lewiso teorija. Rūgštinių anijonų stabilumas yra kokybinis rūgštinių savybių rodiklis. Rūgštinių ar bazinių savybių pokyčių bendrieji modeliai, palyginti su rūgščių ar bazinių centrų atomų pobūdžiu, elektroninis pakaitų poveikis šiuose centruose. Organinių junginių, turinčių vandenilio turinčių funkcinių grupių, rūgštinės savybės (alkoholiai, fenoliai, tioliai, karboksirūgštys, aminai, molekulių СН-rūgštingumas ir kabbracijos). p-pagrindai ir n-pamatai. Pagrindinės neutralių molekulių, turinčių heteroatomų, savybės su vienišų elektronų poromis (alkoholiais, tioliais, sulfidais, aminais) ir anijonais (hidroksido, alkoksido jonais, organinių rūgščių anijonais). Azoto turinčių heterociklų (pirolio, imidazolo, piridino) rūgščių ir šarmų savybės. Vandenilio ryšys kaip specifinis rūgščių ir šarmų savybių pasireiškimas.
Junginių, turinčių hidroksilo grupę, rūgščių savybių lyginamosios charakteristikos (vienvandeniai ir daugiasluoksniai alkoholiai, fenoliai, karboksirūgštys) Alifatinių ir aromatinių aminų pagrindinių savybių lyginamosios charakteristikos. Pakaito elektroninio pobūdžio įtaka organinių molekulių rūgščių ir šarmų savybėms.
Kompetencijos reikalavimai:
· Žinoti rūgščių ir bazių apibrėžimus pagal Bronstedo protolitinę teoriją ir elektroninę Lewiso teoriją.
· Žinoti Bronstedo rūgščių ir bazių klasifikaciją, atsižvelgiant į rūgštinių ar bazinių centrų atomų pobūdį.
· Žinoti veiksnius, turinčius įtakos rūgščių stiprumui ir joms konjuguotų bazių stabilumui, mokėti atlikti lyginamąjį rūgščių stiprumo įvertinimą, remiantis atitinkamų anijonų stabilumu
· Žinoti veiksnius, turinčius įtakos Bronstedo bazių stiprumui, mokėti atlikti lyginamąjį bazių stiprumo įvertinimą, atsižvelgiant į šiuos veiksnius.
· Žinoti vandenilio jungčių atsiradimo priežastis, mokėti interpretuoti vandenilio jungčių susidarymą kaip specifinį medžiagos rūgščių ir šarmų savybių pasireiškimą.
· Žinoti keto-enolio tautomerizmo atsiradimo priežastis organinėse molekulėse, mokėti jas paaiškinti junginių rūgščių ir šarmų savybių požiūriu, atsižvelgiant į jų biologinį aktyvumą.
· Žinoti ir mokėti atlikti aukštos kokybės reakcijas, leidžiančias atskirti daugiasluoksnius alkoholius, fenolius, tiolius.
4 tema. Nukleofilinio pakaitalo reakcijos tetragoniame anglies atome ir konkurencinės eliminacijos reakcijos
Nukleofilinio pakaitalo reakcijos prie hibridizuoto sp3 anglies atomo: heterolitinės reakcijos dėl anglies ir heteroatomo jungties poliarizacijos (halogeno dariniai, alkoholiai). Lengvas ir sunkus pasitraukimas iš grupių: santykis tarp lengvumo išeiti iš grupės ir jos struktūros. Tirpiklių, elektroninių ir erdvinių veiksnių įtaka junginių reaktyvumui mono- ir bimolekulinės nukleofilinės pakaitos (SN1 ir SN2) reakcijose. Nukleofilinių pakaitų reakcijų stereochemija.
Halogeno darinių hidrolizės reakcijos. Alkoholių, fenolių, tiolių, sulfidų, amoniako, aminų alkilinimo reakcijos. Rūgščių katalizės vaidmuo nukleofiliniame pakaitale hidroksilo grupė... Halogeninti dariniai, alkoholiai, sieros ir fosforo rūgščių esteriai kaip alkilinantys reagentai. Biologinis alkilinimo reakcijų vaidmuo.
Mono- ir bimolekulinės eliminacijos (E1 ir E2) reakcijos: (dehidracija, dehidrohalogeninimas). Padidėjęs CH rūgštingumas yra pašalinimo reakcijų, lydinčių nukleofilinį pakaitalą sp3 hibridizuoto anglies atomo, priežastis.
Kompetencijos reikalavimai:
· Žinoti veiksnius, lemiančius reagentų nukleofilumą, svarbiausių nukleofilinių dalelių struktūrą.
· Žinoti nukleofilinių pakaitų reakcijų prie prisotinto anglies atomo bendrus modelius, statinių ir dinaminių veiksnių įtaką medžiagos reaktyvumui nukleofilinių pakaitų reakcijoje.
· Žinoti mono- ir bimolekulinės nukleofilinės pakaitos mechanizmus, mokėti įvertinti sterinių veiksnių, tirpiklių įtaką, statinių ir dinaminių veiksnių įtaką reakcijos eigai pagal vieną iš mechanizmų.
· Žinoti mono- ir bimolekulinės eliminacijos mechanizmus, konkurencijos tarp nukleofilinio pakaitalo ir eliminacijos priežastis.
· Žinoti Zaicevo taisyklę ir mokėti nustatyti pagrindinį produktą nesimetriškų alkoholių ir halogenintų alkanų dihidracijos ir dehidrohalogeninimo reakcijose.
5 tema. Nukleofilinio prisijungimo ir pakeitimo reakcijos prie trigoninio anglies atomo
Nukleofilinės adicijos reakcijos: heterolitinės reakcijos, susijusios su anglies ir deguonies p jungtimi (aldehidai, ketonai). Karbonilo junginių sąveikos su nukleofiliniais reagentais (vandeniu, alkoholiais, tiolais, aminais) reakcijų mechanizmas. Elektroninių ir erdvinių veiksnių įtaka, rūgščių katalizės vaidmuo, nukleofilinių prisijungimo reakcijų grįžtamumas. Pusiau acetaliai ir acetalai, jų paruošimas ir hidrolizė. Biologinis acetalizacijos reakcijų vaidmuo. Aldolio pridėjimo reakcijos. Pagrindinė katalizė. Enolato - jono struktūra.
Karboksirūgščių serijos nukleofilinės pakaitinės reakcijos. Elektroninė ir erdvinė karboksilo grupės struktūra. Nukleofilinio pakaitalo reakcijos prie hibridizuoto sp2 anglies atomo (karboksirūgštys ir jų funkciniai dariniai). Acilinantys agentai (halogenidai, anhidridai, karboksirūgštys, esteriai, amidai), jų reaktyvumo lyginamosios charakteristikos. Acilinimo reakcijos - anhidridų, esterių, tioesterių, amidų susidarymas ir jų atvirkštinės hidrolizės reakcijos. Acetilkoenzimas A yra natūralus didelės energijos acilinimo agentas. Biologinis acilinimo reakcijų vaidmuo. Nukleofilinio pakaitalo prie fosforo atomų samprata, fosforilinimo reakcijos.
Organinių junginių oksidacijos ir redukcijos reakcijos. Organinių junginių redoksinių reakcijų specifiškumas. Vieno elektrono perdavimo, hidrido jonų perdavimo samprata ir NAD + ↔ NADH sistemos veikimas. Alkoholių, fenolių, sulfidų, karbonilo junginių, aminų, tiolių oksidacijos reakcijos. Karbonilo junginių, disulfidų redukcijos reakcijos. Redokso reakcijų vaidmuo gyvenimo procesuose.
Kompetencijos reikalavimai:
· Žinoti elektroninę ir erdvinę karbonilo grupės struktūrą, elektroninių ir sterinių veiksnių įtaką okso grupės reaktyvumui aldehiduose ir ketonuose.
· Žinoti vandens, alkoholių, aminų, tiolių nukleofilinio prisijungimo prie aldehidų ir ketonų reakcijų mechanizmą, katalizatoriaus vaidmenį.
· Žinoti aldolio kondensacijos reakcijų mechanizmą, veiksnius, lemiančius junginio dalyvavimą šioje reakcijoje.
· Žinoti okso junginių redukcijos metalo hidridais reakcijų mechanizmą.
· Žinokite reakcijos centrus, esančius karboksirūgšties molekulėse. Gebėti palyginti karboksirūgščių stiprumą, atsižvelgiant į radikalo struktūrą.
· Žinoti elektroninę ir erdvinę karboksilo grupės struktūrą, mokėti atlikti lyginamąjį oksogrupės anglies atomo karboksirūgštyse ir jų funkciniuose dariniuose (halogenidai, anhidridai, esteriai, amidai, druskos) gebėjimą patirti nukleofilinę ataką.
· Žinoti nukleofilinių pakaitų reakcijų mechanizmus pagal acilinimo, esterinimo, esterių, anhidridų, halogenidų, amidų pavyzdžius.
6 tema. Lipidai, klasifikacija, struktūra, savybės
Lipidai yra muilinami ir nemuilinami. Neutralūs lipidai. Natūralūs riebalai kaip triacilglicerolių mišinys. Pagrindinės natūralios aukštosios riebalų rūgštys, sudarančios lipidus, yra palmitinas, stearinas, oleinas, linolo rūgštis, linolenas. Arachidono rūgštis. Nesočiųjų savybės riebalų rūgštys, w-nomenklatūra.
Nesočiųjų riebalų rūgščių fragmentų peroksidacija ląstelių membranose. Membraninės lipidų peroksidacijos vaidmuo veikiant mažas radiacijos dozes kūnui. Antioksidacinės gynybos sistemos.
Fosfolipidai. Fosfatidinės rūgštys. Fosfatidilkolaminai ir fosfatidilserinai (cefalinai), fosfatidilcholinai (lecitinai) yra struktūriniai ląstelių membranų komponentai. Lipidų bisluoksnis. Sfingolipidai, keramidai, sfingomielinai. Smegenų glikolipidai (cerebrozidai, gangliozidai).
Kompetencijos reikalavimai:
· Žinoti lipidų klasifikaciją, jų struktūrą.
· Žinoti muilinamų lipidų struktūrinių komponentų - alkoholių ir aukštesnių riebalų rūgščių - struktūrą.
· Žinoti paprastų ir sudėtingų lipidų susidarymo ir hidrolizės reakcijų mechanizmą.
· Žinoti ir mokėti atlikti kokybines reakcijas į nesočiąsias riebalų rūgštis ir aliejus.
· Žinoti nemuilinamų lipidų klasifikaciją, suvokti terpenų ir steroidų klasifikavimo principus, jų biologinį vaidmenį.
· Žinoti biologinį lipidų vaidmenį, jų pagrindines funkcijas, suvokti pagrindinius lipidų peroksidacijos etapus ir šio proceso pasekmes ląstelei.
2 skyrius. Organinių molekulių stereoizomerizmas. Daugiafunkciniai ir heterofunkciniai junginiai, dalyvaujantys gyvybiškai svarbiuose procesuose
7 tema. Organinių molekulių stereoizomerizmas
Stereoizomerizmas junginių su dvigubu ryšiu serijoje (p-diastereomerizmas). Nesočiųjų junginių cis ir trans izomerija. E, Z - p-diastereomerų žymėjimo sistema. Lyginamasis p-diastereomerų stabilumas.
Chiralinės molekulės. Asimetriškas anglies atomas kaip chiralijos centras. Molekulių, turinčių vieną chirališkumo centrą, stereoizomerizmas (enantiomerizmas). Optinė veikla. Fišerio projekcijos formulės. Glicerino aldehidas kaip konfigūracijos standartas, absoliuti ir santykinė konfigūracija. D, L stereocheminės nomenklatūros sistema. R, S-stereochemijos nomenklatūros sistema. Rasiniai mišiniai ir jų atskyrimo metodai.
Molekulių, turinčių du ar daugiau chiralinių centrų, stereoizomerizmas. Enantiomerai, diastereomerai, mezoformos.
Kompetencijos reikalavimai:
· Žinoti stereoizomerizmo atsiradimo priežastis alkenų ir dieno angliavandenilių serijose.
· Gebėti nustatyti p-diastereomerų egzistavimo galimybę pagal nesočiųjų junginių sumažintą struktūrinę formulę, išskirti cis-trans-izomerus, įvertinti jų lyginamąjį stabilumą.
· Žinoti molekulių simetrijos elementus, būtinas sąlygas chirališkumui atsirasti organinėje molekulėje.
Žinoti ir mokėti pavaizduoti naudojant enantiomerus projekcijos formulės Fišeris, norėdamas apskaičiuoti laukiamų stereoizomerų skaičių, remdamasis chiralinių centrų skaičiumi molekulėje, stereocheminės nomenklatūros absoliučios ir santykinės konfigūracijos, D-, L-sistemos nustatymo principais.
· Žinoti racematų atskyrimo būdus, pagrindinius stereocheminės nomenklatūros R, S sistemos principus.
8 tema. Fiziologiškai aktyvūs alifatinių, aromatinių ir heterociklinių serijų poli - ir heterofunkciniai junginiai
Poli- ir heterofunkcionalumas kaip vienas iš būdingi bruožai organiniai junginiai, dalyvaujantys gyvybiškai svarbiuose procesuose ir būdami svarbiausių narkotikų grupių protėviai. Funkcinių grupių tarpusavio įtakos, atsižvelgiant į jų santykinę vietą, ypatybės.
Polihidroksiliai alkoholiai: etilenglikolis, glicerinas. Daugiabučių alkoholių esteriai su neorganinėmis rūgštimis (nitroglicerinu, glicerino fosfatais). Diatominiai fenoliai: hidrochinonas. Diatominių fenolių oksidavimas. Hidrochinono-chinono sistema. Fenoliai kaip antioksidantai (laisvųjų radikalų valikliai). Tokoferoliai.
Dvibazės karboksirūgštys: oksalo, malono, gintaro, glutaro, fumaro. Gintaro rūgšties pavertimas fumaro rūgštimi kaip biologiškai svarbios dehidrinimo reakcijos pavyzdys. Dekarboksilinimo reakcijos, jų biologinis vaidmuo.
Amino alkoholiai: aminoetanolis (kolaminas), cholinas, acetilcholinas. Acetilcholino vaidmuo vykstant cheminiam nervinių impulsų perdavimui sinapsėse. Aminofenoliai: dopaminas, norepinefrinas, adrenalinas. Šių junginių ir jų darinių biologinio vaidmens samprata. Neurotoksinis 6-hidroksidopamino ir amfetaminų poveikis.
Hidroksi ir amino rūgštys. Ciklizacijos reakcijos: įtaka įvairūs veiksniai apie ciklų susidarymo procesą (atitinkamų konformacijų įgyvendinimas, suformuoto ciklo dydis, entropijos faktorius). Laktonai. Laktamai. Laktonų ir laktamų hidrolizė. B-hidroksi ir amino rūgščių pašalinimo reakcija.
Aldehido ir keto rūgštys: piruvinė, acetoacto, oksaloacto, a-ketoglutaro. Rūgštinės savybės ir reaktyvumas... B-keto rūgščių dekarboksilinimo ir a-keto rūgščių oksidacinio dekarboksilinimo reakcijos. Acetoacto eteris, keto-enolio tautomerizmas. „Ketoninių kūnų“ atstovai yra b-hidroksibutiras, b-ketobutirūgštis, acetonas, jų biologinė ir diagnostinė reikšmė.
Heterofunkciniai benzolo serijos dariniai kaip vaistai. Salicilo rūgštis ir jos dariniai (acetilsalicilo rūgštis).
Para-aminobenzenkarboksirūgštis ir jos dariniai (anestezinas, novokainas). Biologinis p-aminobenzenkarboksirūgšties vaidmuo. Sulfanilo rūgštis ir jos amidas (streptocidas).
Heterociklai su keliais heteroatomais. Pirazolas, imidazolas, pirimidinas, purinas. Pirazolonas-5 yra ne narkotinių analgetikų pagrindas. Barbitūro rūgštis ir jos dariniai. Hidroksipurinai (hipoksantinas, ksantinas, šlapimo rūgštis), jų biologinis vaidmuo. Heterociklai su vienu heteroatomu. Pirolis, indolis, piridinas. Biologiškai svarbūs piridino dariniai - nikotinamidas, piridoksalas, izonikotino rūgšties dariniai. Nikotinamidas yra struktūrinis kofermento NAD + komponentas, nulemiantis jo dalyvavimą OVR.
Kompetencijos reikalavimai:
· Gebėti klasifikuoti heterofunkcinius junginius pagal jų sudėtį ir tarpusavio išsidėstymą.
· Žinoti specifines amino ir hidroksirūgščių reakcijas su a, b, g - funkcinių grupių išsidėstymą.
· Žinoti reakcijas, sukeliančias biologiškai aktyvių junginių susidarymą: cholino, acetilcholino, adrenalino.
· Žinoti keto-enolio tautomerizmo vaidmenį pasireiškiant keto rūgščių (piruvinio, oksaloacto, acetoacto) ir heterociklinių junginių (pirazolo, barbitūro rūgšties, purino) biologiniam aktyvumui.
· Žinoti organinių junginių redoksinių transformacijų metodus, redoksinių reakcijų biologinį vaidmenį pasireiškiant diatominių fenolių, nikotinamido biologiniam aktyvumui, formuojantis ketoniniams kūnams.
Tema9 . Angliavandeniai, klasifikacija, struktūra, savybės, biologinis vaidmuo
Angliavandeniai, jų klasifikacija hidrolizės atžvilgiu. Monosacharidų klasifikacija. Aldozės, ketozės: triozės, tetozės, pentozės, heksozės. Monosacharidų stereoizomerizmas. D ir L serijos stereocheminės nomenklatūros. Atviros ir cikliškos formos. Fišerio formulės ir „Hewors“ formulės. Furanozė ir piranozė, a - ir b - anomerai. Ciklo-okso-tautomerizmas. Monosacharidų piranozės formų konformacija. Svarbiausių pentozių atstovų (ribozės, ksilozės) struktūra; heksozė (gliukozė, manozė, galaktozė, fruktozė); dezoksi cukrūs (2-dezoksiribozė); amino cukrų (gliukozaminas, mannosaminas, galaktozaminas).
Cheminės monosacharidų savybės. Nukleofilinės pakaitinės reakcijos, susijusios su anomeriniu centru. O ir N-glikozidai. Glikozidų hidrolizė. Monosacharidų fosfatai. Monosacharidų oksidavimas ir redukcija. Regeneracinės aldozių savybės. Glikono, glikaro, glikurono rūgštys.
Oligosacharidai. Disacharidai: maltozė, celobiozė, laktozė, sacharozė. Struktūra, ciklo-okso-tautomerizmas. Hidrolizė.
Polisacharidai. Bendrosios polisacharidų charakteristikos ir klasifikacija. Homo- ir heteropolisacharidai. Homopolisacharidai: krakmolas, glikogenas, dekstranai, celiuliozė. Pirminė struktūra, hidrolizė. Antrinės struktūros samprata (krakmolas, celiuliozė).
Kompetencijos reikalavimai:
Žinoti monosacharidų klasifikaciją (pagal anglies atomų skaičių, funkcinių grupių sudėtį), svarbiausių monosacharidų atvirų ir ciklinių formų (furanozės, piranozės) struktūrą, jų santykį su stereocheminės nomenklatūros D ir L serijomis, mokėti nustatyti galimų diastereomerų skaičių, stereoizomerus nukreipti į diastereomus , epimerai, anomerai.
· Žinoti monosacharidų ciklimizacijos reakcijų mechanizmą, monosacharidų tirpalų mutarotacijos priežastis.
· Žinoti monosacharidų chemines savybes: redokso reakcijas, O ir N-glikozidų susidarymo ir hidrolizės reakcijas, esterinimo, fosforilinimo reakcijas.
· Gebėti atlikti kokybines reakcijas į diolio fragmentą ir monosacharidų redukcinių savybių buvimą.
· Žinoti disacharidų klasifikaciją ir jų struktūrą, glikozidinį ryšį formuojančio anomerinio anglies atomo konfigūraciją, disacharidų tautomerines transformacijas, jų chemines savybes, biologinį vaidmenį.
· Žinoti polisacharidų klasifikaciją (atsižvelgiant į hidrolizę, pagal monosacharidų sudėtį), svarbiausių homopolisacharidų atstovų struktūrą, glikozidinį ryšį formuojančio anomero anglies atomo konfigūraciją, jų fizines ir chemines savybes bei biologinį vaidmenį. Suprasti heteropolisacharidų biologinį vaidmenį.
10 tema.a-Aminorūgštys, peptidai, baltymai. Struktūra, savybės, biologinis vaidmuo
A-aminorūgščių, sudarančių baltymus ir peptidus, struktūra, nomenklatūra, klasifikacija. A-aminorūgščių stereoizomerizmas.
Biosintetiniai keliai, skirti susidaryti a-aminorūgštims iš okso rūgščių: redukcinės aminavimo ir transaminacijos reakcijos. Nepakeičiamos amino rūgštys.
Cheminės a-aminorūgščių, kaip heterofunkcinių junginių, savybės. A-aminorūgščių rūgščių ir šarmų savybės. Izoelektrinis taškas, a-aminorūgščių atskyrimo metodai. Intrakompleksinių druskų susidarymas. Esterinimo, acilinimo, alkilinimo reakcijos. Sąveika su azoto rūgštimi ir formaldehidu, šių reakcijų svarba analizuojant aminorūgštis.
g-amino sviesto rūgštis yra centrinę nervų sistemą slopinantis tarpininkas. Antidepresinis L-triptofano, serotonino poveikis - kaip miego neuromediatorius. Tarpinės glicino, histamino, asparto ir glutamo rūgščių savybės.
Biologiškai svarbios a-aminorūgščių reakcijos. Deamininimo ir hidroksilinimo reakcijos. A-aminorūgščių dekarboksilinimas - kelias į biogeninių aminų ir bioreguliatorių (kolamino, histamino, triptamino, serotonino.) Peptidų susidarymą. Elektroninė peptidinio ryšio struktūra. Rūgštinė ir šarminė peptidų hidrolizė. Aminorūgščių sudėties nustatymas naudojant šiuolaikinius fizikocheminius metodus (Sangerio ir Edmano metodus). Neuropeptidų samprata.
Pagrindinė baltymų struktūra. Dalinė ir visiška hidrolizė. Antrinių, tretinių ir ketvirtinių struktūrų samprata.
Kompetencijos reikalavimai:
· Žinoti a-aminorūgščių, priklausančių natūralių aminorūgščių, nepakeičiamų aminorūgščių D ir L stereocheminėms serijoms, struktūrą, stereocheminę klasifikaciją.
· Žinoti a-aminorūgščių sintezės būdus in vivo ir in vitro, žinoti rūgščių-šarmų savybes ir metodus, kaip paversti a-aminorūgštis izoelektrine būsena.
· Žinoti a-aminorūgščių chemines savybes (reakcijos į amino ir karboksilo grupes), mokėti atlikti kokybines reakcijas (ksantoproteinas, su Cu (OH) 2, ninhidrinu).
· Žinoti peptidinio ryšio elektroninę struktūrą, pirminę, antrinę, tretinę ir ketvirtinę baltymų ir peptidų struktūrą, mokėti nustatyti aminorūgščių sudėtį ir aminorūgščių seką (Sengerio metodas, Edmano metodas), mokėti atlikti peptidų ir baltymų biureto reakciją.
· Žinoti peptidų sintezės metodo principą, naudojant funkcinių grupių apsaugą ir aktyvavimą.
11 tema. Nukleotidai ir nukleorūgštys
Nukleorūgštys, iš kurių susidaro nukleorūgštys. Pirimidino (uracilo, timino, citozino) ir purino (adenino, guanino) bazės, jų aromatiškumas, tautomerinės transformacijos.
Nukleozidai, jų susidarymo reakcijos. Ryšio tarp nukleorūgšties bazės ir angliavandenių liekanos pobūdis; glikozidinio centro konfigūracija. Nukleozidų hidrolizė.
Nukleotidai. Nukleorūgštis sudarančių mononukleotidų struktūra. Nomenklatūra. Nukleotidų hidrolizė.
Pirminė nukleorūgščių struktūra. Fosfodiesterio ryšys. Ribonukleino ir dezoksiribonukleino rūgštys. RNR ir DNR nukleotidų sudėtis. Nukleino rūgšties hidrolizė.
Antrinės DNR struktūros samprata. Vandenilio ryšių vaidmuo formuojant antrinę struktūrą. Nukleinės bazės papildomumas.
Vaistai, kurių pagrindas yra modifikuotos nukleorūgšties bazės (5-fluorouracilas, 6-merkaptopurinas). Cheminio panašumo principas. Nukleorūgščių struktūros pokyčiai veikiant chemikalams ir radiacijai. Azoto rūgšties mutageninis poveikis.
Nukleozidiniai polifosfatai (ADP, ATP), jų struktūros ypatumai, leidžiantys jiems atlikti didelės energijos junginių ir tarpląstelinių bioreguliatorių funkcijas. CAMP struktūra - viduląstelinis hormonų „tarpininkas“.
Kompetencijos reikalavimai:
· Žinoti pirimidino ir purino azoto bazių struktūrą, jų tautomerines transformacijas.
· Žinoti N-glikozidų (nukleozidų) susidarymo reakcijų mechanizmą ir jų hidrolizę, nukleozidų nomenklatūrą.
· Žinoti pagrindinius natūralių ir sintetinių antibiotikų nukleozidų panašumus ir skirtumus, palyginti su nukleozidais, kurie yra DNR ir RNR dalis.
· Žinoti nukleotidų susidarymo reakcijas, mononukleotidų, sudarančių nukleorūgštis, struktūrą, jų nomenklatūrą.
· Žinoti nukleozidų ciklo- ir polifosfatų struktūrą, jų biologinį vaidmenį.
· Žinoti DNR ir RNR nukleotidų sudėtį, fosfodiesterio ryšio vaidmenį kuriant pirminę nukleorūgščių struktūrą.
· Žinoti vandenilio ryšių vaidmenį formuojant antrinę DNR struktūrą, azoto bazių papildomumą, papildomų sąveikų vaidmenį įgyvendinant biologinę DNR funkciją.
· Žinoti mutacijų atsiradimą lemiančius veiksnius ir jų veikimo principą.
Informacinė dalis
Bibliografija
Pagrindinis:
1. Romanovsky, bioorganinė chemija: 2 dalių vadovėlis /. - Minskas: BSMU, 20 m.
2. Romanovsky, skirtas bioorganinės chemijos seminarui: vadovėlis / redagavo. - Minskas: BSMU, 1999. - 132 p.
3. Tyukavkina, N. A., Bioorganinė chemija: vadovėlis / ,. - Maskva: medicina, 1991. - 528 p.
Papildomas:
4. Ovčinnikovas, chemija: monografija /.
- Maskva: švietimas, 1987. - 815 p.
5. Potapovas,: pamoka /. - Maskva:
Chemija, 1988. - 464 p.
6. Riles, A. Organinės chemijos pagrindai: pamoka / A. Rice, K. Smith,
R. Wardas. - Maskva: Mir, 1989. - 352 p.
7. Taylor, G. Organinės chemijos pagrindai: pamoka / G. Taylor. -
Maskva: Mearsas.
8. Terney, A. Šiuolaikinė organinė chemija: 2 tomų vadovėlis /
A. Terney. - Maskva: Mir, 1981. - 1310 p.
9. Tyukavkina, už bioorganinių medžiagų laboratorinius tyrimus
chemija: vadovėlis / [ir kiti]; redagavo N.A.
Tyukavkina. - Maskva: medicina, 1985 m. - 256 p.
10. Tyukavkina, N. A., Bioorganinė chemija: vadovėlis studentams
medicinos institutai / ,. - Maskva.
Planas 1. Bioorganinės chemijos dalykas ir reikšmė 2. Organinių junginių klasifikacija ir nomenklatūra 3. Organinių molekulių atvaizdo metodai 4. Cheminis ryšys bioorganinėse molekulėse 5. Elektroniniai efektai. Abipusė molekulių atomų įtaka 6. Cheminių reakcijų ir reagentų klasifikacija 7. Cheminių reakcijų mechanizmų samprata 2

Bioorganinės chemijos tema 3 Bioorganinė chemija yra savarankiška chemijos mokslo šaka, tirianti struktūrą, savybes ir biologines funkcijas cheminiai junginiai organinės kilmės, kurios dalyvauja gyvųjų organizmų apykaitoje.

Bioorganinės chemijos tyrimo objektai yra mažos molekulinės masės biomolekulės ir biopolimerai (baltymai, nukleino rūgštys ir polisacharidai), bioreguliatoriai (fermentai, hormonai, vitaminai ir kt.), Natūralūs ir sintetiniai fiziologiškai aktyvūs junginiai, įskaitant vaistus ir toksišką poveikį turinčias medžiagas. Biomolekulės - bioorganiniai junginiai, kurie yra gyvų organizmų dalis ir specializuojasi ląstelių struktūrų formavimuisi ir dalyvavimui biocheminėse reakcijose, sudaro gyvų ląstelių ir apskritai daugialąsčių organizmų metabolizmo (metabolizmo) ir fiziologinių funkcijų pagrindą. 4 Bioorganinių junginių klasifikacija

Metabolizmas yra organizme vykstančių cheminių reakcijų (in vivo) visuma. Metabolizmas dar vadinamas metabolizmu. Metabolizmas gali vykti dviem kryptimis - anabolizmu ir katabolizmu. Anabolizmas yra sudėtingų medžiagų sintezė organizme iš palyginti paprastų. Jis sunaudoja energiją (endoterminis procesas). Katabolizmas - priešingai, sudėtingų organinių junginių skaidymas į paprastesnius. Tai vyksta išsiskiriant energijai (egzoterminis procesas). Metaboliniai procesai vyksta dalyvaujant fermentams. Fermentai atlieka biologinių katalizatorių vaidmenį organizme. Be fermentų biocheminiai procesai arba nevyktų, arba vyktų labai lėtai, o kūnas negalėtų palaikyti gyvybės. penki

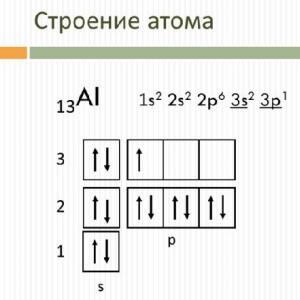
Bioelementai. Be anglies atomų (C), kurie sudaro bet kurios organinės molekulės pagrindą, bioorganinių junginių sudėtyje taip pat yra vandenilis (H), deguonis (O), azotas (N), fosforas (P) ir siera (S). Šie bioelementai (organogenai) yra koncentruoti gyvuose organizmuose daugiau nei 200 kartų viršijančių jų kiekį negyvuose objektuose. Pažymėti elementai sudaro daugiau kaip 99% elementinės biomolekulių sudėties. 6


Bioorganinė chemija atsirado iš organinės chemijos gelmių ir yra pagrįsta jos idėjomis bei metodais. Organinės chemijos raidos istorijoje priskiriami šie etapai: empiriniai, analitiniai, struktūriniai ir šiuolaikiniai. Laikotarpis nuo pirmojo žmogaus pažinties su organinėmis medžiagomis iki XVIII amžiaus pabaigos laikomas empiriniu. Pagrindinis šio laikotarpio rezultatas yra tai, kad žmonės suprato elementų analizės ir atominės bei molekulinės masės nustatymo svarbą. Vitalizmo teorija - gyvybės jėga (Berzelius). Analitinis laikotarpis truko iki XXX amžiaus 60-ųjų. Tai pasižymėjo tuo, kad nuo XIX amžiaus pirmojo ketvirčio pabaigos buvo padaryta daugybė perspektyvių atradimų, kurie suteikė triuškinantį smūgį vitalistinei teorijai. Pirmasis šioje eilėje buvo Berzeliaus mokinys, vokiečių chemikas Wöhleris. 1824 m. Jis padarė daug atradimų - oksalo rūgšties sintezę iš cianogeno: (CN) 2 HOOC - COOH p. - karbamido sintezė iš amonio cianato: NH 4 CNO NH 2 - C - NH 2 O 8

1853 m. C. Gerardas sukūrė „tipų teoriją“ ir panaudojo ją organiniams junginiams klasifikuoti. Pasak Gerardo, sudėtingesnius organinius junginius galima gaminti iš šių keturių pagrindinių medžiagų rūšių: НННН tipo vandenilio devyni

Pagrindinės organinių junginių struktūros teorijos nuostatos (1861) 1) atomai molekulėse yra tarpusavyje sujungiami cheminėmis jungtimis pagal jų valentingumą; 2) organų medžiagų molekulėse esantys atomai yra tarpusavyje susiję tam tikra seka, kuri lemia molekulės cheminę struktūrą (struktūrą); 3) organinių junginių savybės priklauso ne tik nuo juos sudarančių atomų skaičiaus ir pobūdžio, bet ir nuo cheminės molekulių struktūros; 4) organinėse molekulėse yra tarpusavyje susietų ir nesurištų atomų sąveika; 5) cheminę medžiagos struktūrą galima nustatyti tiriant jos cheminius virsmus ir, priešingai, pagal medžiagos struktūrą galima apibūdinti jos savybes. dešimt

Pagrindinės organinių junginių struktūros teorijos nuostatos (1861) Struktūrinė formulė yra atomų ryšių sekos molekulėje vaizdas. Bendroji formulė - CH 4 O arba CH 3 OH Struktūrinė formulė Supaprastintos struktūros formulės kartais vadinamos racionaliomis Molekulinė formulė - organinio junginio formulė, nurodanti kiekvieno elemento atomų skaičių molekulėje. Pvz .: С 5 Н 12 - pentanas, С 6 Н 6 - benzinas ir kt. vienuolika



Bioorganinės chemijos raidos etapai Kaip atskira žinių sritis, apjungianti koncepcinius organinės chemijos principus ir metodiką, viena vertus, ir molekulinę biochemiją bei molekulinę farmakologiją, kita vertus, bioorganinė chemija susiformavo XX a. Metais, remiantis natūralių medžiagų ir biopolimerų chemijos raida. Šiuolaikinė bioorganinė chemija įgijo esminę reikšmę dėka W. Steino, S. Moore'o, F. Sengero (aminorūgščių sudėties analizė ir peptidų bei baltymų pirminės struktūros nustatymas), L. Paulingo ir H. Astbury darbų (-helix ir -structure struktūros ir jų reikšmingumo išaiškinimas). įgyvendinant baltymų molekulių biologines funkcijas), E. Chargaffa (iššifruojantis nukleorūgščių nukleotidų sudėties ypatybes), J. Watsonas, kun. Crickas, M. Wilkinsas, R. Franklinas (nustatantys DNR molekulės erdvinės struktūros dėsnius), G. Korani (cheminė geno sintezė) ir kt. keturiolika

Organinių junginių klasifikavimas pagal anglies skeleto struktūrą ir funkcinės grupės pobūdį Didžiulis organinių junginių skaičius paskatino chemikus juos klasifikuoti. Organinių junginių klasifikacija grindžiama dviem klasifikavimo ypatumais: 1. Anglies griaučių struktūra 2. Funkcinių grupių pobūdis Klasifikavimas pagal anglies griaučių struktūrą: 1. Acikliniai (alkanai, alkenai, alkinai, alkadienai); 2. Ciklinis 2.1. Karbocikliniai (alicikliniai ir aromatiniai) 2.2. Heterocikliniai 15 Acikliniai junginiai taip pat vadinami alifatiniais. Tai apima medžiagas su atvira anglies grandine. Acikliniai junginiai skirstomi į sočiuosius (arba prisotintus) CnH2n + 2 (alkanus, parafinus) ir nesočiuosius (nesočiuosius). Pastarieji apima alkenus C n H 2n, alkinus C n H 2n -2, alkadienus C n H 2n -2.

16 Ciklinių junginių molekulėse yra žiedai (ciklai). Jei ciklai apima tik anglies atomus, tai tokie junginiai vadinami karbocikliniais. Savo ruožtu karbocikliniai junginiai skirstomi į aliciklinius ir aromatinius. Alicikliniai angliavandeniliai (cikloalkanai) apima ciklopropaną ir jo homologus - ciklobutaną, ciklopentaną, cikloheksaną ir kt. Jei, be angliavandenilio, į ciklinę sistemą patenka ir kiti elementai, tai tokie junginiai vadinami heterocikliniais.

Klasifikavimas pagal funkcinės grupės pobūdį Funkcinė grupė yra tam tikru būdu surištas atomas arba atomų grupė, kurios buvimas organinės medžiagos molekulėje lemia būdingąsias savybes ir jos priklausymą vienai ar kitai junginių klasei. Pagal funkcinių grupių skaičių ir homogeniškumą organiniai junginiai skirstomi į mono-, poli- ir heterofunkcinius. Medžiagos, turinčios vieną funkcinę grupę, vadinamos monofunkcinėmis, turinčiomis kelias identiškas funkcines grupes, daugiafunkcinėmis. Junginiai, turintys kelias skirtingas funkcines grupes, yra hetero funkciniai. Svarbu, kad tos pačios klasės junginiai būtų sujungti į homologines serijas. Homologinė serija yra organinių junginių, turinčių tas pačias funkcines grupes ir tą pačią struktūrą, serija, kiekvienas homologinės serijos atstovas nuo ankstesnės skiriasi pastoviu vienetu (CH 2), kuris vadinamas homologiniu skirtumu. Homologinės serijos nariai vadinami homologais. 17

Organinės chemijos nomenklatūros sistemos - triviali, racionali ir tarptautinė (IUPAC) cheminė nomenklatūra - atskirų cheminių medžiagų pavadinimų rinkinys, jų grupės ir klasės, taip pat jų pavadinimų sudarymo taisyklės. Cheminė nomenklatūra - atskirų cheminių medžiagų, jų grupių ir klasių pavadinimų rinkinys, taip pat taisyklės rengiant jų vardus. Trivialioji (istorinė) nomenklatūra siejama su medžiagų gavimo procesu (pirogalolis yra galo rūgšties pirolizės produktas), kilmės šaltiniu, iš kurio ji gauta (skruzdžių rūgštimi) ir kt. Trivialūs junginių pavadinimai plačiai naudojami natūralių ir heterociklinių junginių chemijoje (citralis, geraniolis, tiofenas, pirolis, chinolinas ir kt.). Trivialioji (istorinė) nomenklatūra yra susijusi su medžiagų (pirogalolis yra galo rūgšties pirolizės produktas) gavimo procesu, iš kurio gaunamas šaltinis. kuri buvo gauta (skruzdžių rūgštis) ir kt. Trivialūs junginių pavadinimai plačiai naudojami natūralių ir heterociklinių junginių chemijoje (citralas, geraniolis, tiofenas, pirolis, chinolinas ir kt.). Racionalioji nomenklatūra remiasi organinių junginių padalijimo į homologines serijas principu. Visos tam tikros homologinės serijos medžiagos yra laikomos paprasčiausio tam tikros serijos atstovo - pirmosios arba kartais antrosios - dariniais. Visų pirma, alkanams - metanui, alkenams - etilenui ir kt. Racionalioji nomenklatūra remiasi organinių junginių padalijimo į homologines serijas principu. Visos tam tikros homologinės serijos medžiagos laikomos paprasčiausio tam tikros serijos atstovo dariniais - pirmuoju arba kartais antruoju. Visų pirma, alkanams - metanas, alkenams - etilenas ir kt. aštuoniolika

Tarptautinė nomenklatūra (IUPAC). Šiuolaikinės nomenklatūros taisyklės buvo sukurtos 1957 m. 19-ajame Tarptautinės grynosios ir taikomosios chemijos sąjungos (IUPAC) kongrese. Radikaliai funkcinė nomenklatūra. Šie pavadinimai yra pagrįsti funkcinės klasės pavadinimu (alkoholis, eteris, ketonas ir kt.), Prieš kurį nurodomi angliavandenilių radikalų pavadinimai, pavyzdžiui: alyilo chloridas, dietileteris, dimetilketonas, propilo alkoholis ir kt. Pavaduojanti nomenklatūra. Nomenklatūros taisyklės. Pagrindinė struktūra yra molekulės (molekulinio pagrindo) struktūrinis fragmentas, kuriuo grindžiamas junginio pavadinimas, pagrindinė aliciklinių junginių atomų anglies grandinė, karbociklinių junginių - ciklas. 19

Cheminis ryšys organinėse molekulėse Cheminis ryšys yra išorinių elektronų apvalkalų (atomų valentinių elektronų) ir atomų branduolių sąveikos reiškinys, nulemiantis visos molekulės ar kristalo egzistavimą. Paprastai atomas, priimdamas, dovanodamas elektroną arba formuodamas bendrą elektronų porą, linkęs įgyti išorinio elektrono apvalkalo konfigūraciją, panašią į inertinių dujų. Organiniams junginiams būdingi šie cheminių ryšių tipai: - joninis ryšys - kovalentinis ryšys - donoras - akceptorius - vandenilio ryšys Taip pat yra ir kitų tipų cheminis ryšys (metaliniai, vieno elektrono, dviejų elektronų trijų centrų), tačiau organiniuose junginiuose jų praktiškai nėra. 20



Organinių junginių ryšių tipai Organiniams junginiams būdingiausia kovalentinė jungtis. Kovalentinis ryšys yra atomų sąveika, kuri realizuojama formuojant bendrą elektronų porą. Šio tipo ryšys susidaro tarp atomų, turinčių panašias elektronegatyvumo vertes. Elektronegatyvumas yra atomo savybė, rodanti gebėjimą pritraukti elektronus į save iš kitų atomų. Kovalentinis ryšys gali būti polinis arba nepolinis. Nepolinis kovalentinis ryšys atsiranda tarp atomų, turinčių tą pačią elektronegatyvumo vertę

Organinių junginių ryšių tipai Kovalentinis polinis ryšys susidaro tarp atomų, turinčių skirtingą elektronegatyvumo vertę. Šiuo atveju surišti atomai įgyja dalinius krūvius δ + δ + δ-δ- Ypatingas kovalentinių ryšių potipis yra donoro ir akceptoriaus ryšys. Kaip ir ankstesniuose pavyzdžiuose, tokio tipo sąveika atsiranda dėl bendros elektronų poros buvimo, tačiau pastarąją teikia vienas iš ryšį formuojančių atomų (donoras), o kitas atomas (akceptorius) 24

Organinių junginių ryšių tipai Joninis ryšys susidaro tarp atomų, kurie labai skiriasi savo elektronegatyvumo vertėmis. Šiuo atveju mažiau elektronegatyvaus elemento (dažnai metalo) elektronas visiškai pereina į labiau elektronegatyvų elementą. Šis elektrono perėjimas sukelia teigiamo krūvio atsiradimą mažiau elektronegatyviniame atome, o neigiamą - labiau elektronegatyviniame. Taigi susidaro du priešingų krūvių jonai, tarp kurių vyksta elektrovalentinė sąveika. 25

Organinių junginių ryšių tipai Vandenilio ryšys yra elektrostatinė sąveika tarp vandenilio atomo, kurį jungia stiprus polinis ryšys, ir deguonies, fluoro, azoto, sieros ir chloro elektronų garų. Šis sąveikos tipas yra gana silpna sąveika. Vandenilio ryšys gali būti tarpmolekulinis ir intramolekulinis. Tarpmolekulinis vandenilio ryšys (dviejų etilo alkoholio molekulių sąveika) Intramolekulinis vandenilio ryšys salicilo aldehide 26

Cheminis ryšys organinėse molekulėse Šiuolaikinė cheminio sujungimo teorija remiasi kvantiniu mechaniniu molekulės, kaip sistemos, susidedančios iš elektronų ir atomų branduolių, modeliu. Kvantinės mechaninės teorijos kertinis akmuo yra atominė orbita. Atominė orbita yra erdvės dalis, kurioje elektronų radimo tikimybė yra didžiausia. Todėl ryšys gali būti laikomas orbitalių, pernešančių vieną elektroną su priešingais sukimais, sąveika („sutampa“). 27

Atominių orbitalių hibridizacija Pagal kvantinės mechanikos teoriją, atomo suformuotų kovalentinių ryšių skaičius nustatomas pagal vieno elektrono atominių orbitalių skaičių (nesuporuotų elektronų skaičių). Anglies atomas pagrindinėje būsenoje turi tik du neporinius elektronus, tačiau galimas elektrono perėjimas nuo 2s iki 2pz sukelia keturių kovalentinių ryšių susidarymą. Anglies atomo, kuriame yra keturi neporiniai elektronai, būsena vadinama „sužadinta“. Nepaisant to, kad anglies orbitalės yra nevienodos, yra žinoma, kad keturios lygiavertės jungtys gali susidaryti dėl atominių orbitalių hibridizacijos. Hibridizacija yra reiškinys, kai vienodas tos pačios formos ir skaičiaus orbitalių skaičius susidaro iš kelių skirtingų formų ir artimųjų energijos orbitalių. 28



Hibridinės anglies atomo būsenos organinėse molekulėse PIRMOSIOS HIBRIDINĖS BŪKLĖS C atomas yra sp 3 -hibridizacijos būsenoje, sudaro keturias σ-jungtis, sudaro keturias hibridines orbitales, kurios yra išdėstytos tetraedro (jungties kampo) σ-jungties pavidalu 31

Hibridinės anglies atomo būsenos organinėse molekulėse ANTRA HIBRIDINĖ BŪKLĖ C atomas yra sp 2 būsenoje - hibridizuojantis, suformuoja tris σ ryšius, suformuoja tris hibridines orbitales, kurios išsidėsčiusios plokščio trikampio pavidalu (jungties kampas 120) σ - ryšys π - ryšys 32

Hibridinės anglies atomo būsenos organinėse molekulėse TREČIOSIOS HIBRIDINĖS BŪKLĖS C atomas yra sp hibridizacijos būsenoje, sudaro dvi σ jungtis, sudaro dvi hibridines orbitales, kurios išsidėsčiusios tiesėje (jungties kampas 180)




Cheminių ryšių charakteristikos POLING skalė: F-4,0; O - 3,5; Cl - 3,0; N 3,0; Br 2,8; S - 2,5; C-2,5; H-2.1. skirtumas 1.7
Cheminių ryšių charakteristikos Ryšio poliarizuotumas yra elektronų tankio pokytis veikiant išorės veiksniams. Obligacijų poliarizuotumas yra elektronų judrumo laipsnis. Padidėjus atomo spinduliui, elektronų poliarizuotumas didėja. Todėl anglies-halogeno jungties poliarizuotumas didėja taip: C-F 
Elektroniniai efektai. Abipusė molekulių atomų įtaka 39 Remiantis šiuolaikinėmis teorinėmis koncepcijomis, organinių molekulių reaktyvumą lemia elektronų debesų poslinkis ir judrumas, kurie sudaro kovalentinį ryšį. Organinėje chemijoje išskiriami du elektronų poslinkių tipai: a) elektronų poslinkiai, atsirandantys -liejimo sistemoje, b) elektroniniai poslinkiai, kuriuos perduoda -sijungimo sistema. Pirmuoju atveju vyksta vadinamasis indukcinis poveikis, antruoju - mezomerinis efektas. Indukcinis efektas yra elektronų tankio persiskirstymas (poliarizacija), atsirandantis dėl elektronegatyvumo skirtumo tarp molekulės atomų ryšių sistemoje. Dėl nereikšmingo jungčių poliarizuotumo, indukcinis poveikis greitai išnyksta ir po 3-4 jungčių beveik neatsiranda.

Elektroniniai efektai. Abipusė atomų įtaka molekulėje 40 Indukcinio efekto koncepciją pristatė K. Ingoldas, kuris taip pat pristatė pavadinimus: –I-efektas, jei pakaitalas sumažina elektronų tankį + I-efektas, kai pakaitalas padidina elektronų tankį. Teigiamą indukcinį poveikį rodo alkilo radikalai (СН 3, C 2H 5 ir kt.). Visi kiti anglimi surišti pakaitai turi neigiamą indukcinį poveikį.

Elektroniniai efektai. Abipusė molekulių atomų įtaka 41 Mezomerinis poveikis yra elektronų tankio persiskirstymas palei konjuguotą sistemą. Konjuguotose sistemose yra organinių junginių molekulių, kuriose pakaitomis jungiasi dvigubos ir viengubos jungtys, arba kai šalia dvigubos jungties yra atomas, kurio p-orbitale yra vieniša elektronų pora. Pirmuoju atveju vyksta - konjugacija, o antruoju - p, - konjugacija. Sujungtos sistemos yra su atvira ir uždara sukabinimo grandine. Tokių junginių pavyzdžiai yra 1,3-butadienas ir benzinas. Šių junginių molekulėse anglies atomai yra sp 2 -hibridizacijos būsenoje ir dėl nehibridinių p-orbitalių sudaro β-jungtis, kurios tarpusavyje persidengia ir sudaro vieną elektronų debesį, tai yra, vyksta konjugacija.

Elektroniniai efektai. Abipusė molekulių atomų įtaka 42 Mesomeriniai efektai yra dviejų tipų - teigiamas mesomerinis poveikis (+ M) ir neigiamas mezomerinis poveikis (-M). Pakaitai, teikiantys p-elektronus konjuguotai sistemai, turi teigiamą mezomerinį poveikį. Tai apima: -O, -S -NH2, -OH, -OR, Hal (halogenus) ir kitus pakaitus, turinčius neigiamą krūvį, arba pavienę elektronų porą. Neigiamas mezomerinis poveikis būdingas pakaitalams, kurie traukia elektronų tankį iš konjuguotos sistemos. Tai apima pakaitus, turinčius daugybę ryšių tarp atomų, turinčių skirtingą elektronegatyvumą: - N02; -SO3H; \u003e C \u003d O; -UNON ir kiti. Mesomerinį efektą grafiškai atspindi sulenkta rodyklė, rodanti elektronų poslinkio kryptį. Skirtingai nuo indukcinio efekto, mesomerinis poveikis nėra užgesęs. Jis perduodamas visiškai per sistemą, neatsižvelgiant į sukabinimo grandinės ilgį. C \u003d O; -UNON ir kiti. Mesomerinį efektą grafiškai atspindi sulenkta rodyklė, rodanti elektronų poslinkio kryptį. Skirtingai nuo indukcinio efekto, mesomerinis poveikis nėra užgesęs. Jis visiškai perduodamas per sistemą, neatsižvelgiant į sukabinimo grandinės ilgį 
Cheminės reakcijos tipai 43 Cheminė reakcija gali būti laikoma reagento ir substrato sąveika. Priklausomai nuo cheminio ryšio molekulėse suskaidymo ir formavimo metodo, organinės reakcijos skirstomos į: a) homolizines b) heterolizines c) molekulines Homolizines arba laisvųjų radikalų reakcijas sukelia homolizinio ryšio skilimas, kai kiekvienam atomui lieka vienas elektronas, tai yra, susidaro radikalai ... Homolizinis plyšimas įvyksta aukštoje temperatūroje, veikiant šviesos kvantui arba katalizei.

Heterolitinės arba joninės reakcijos vyksta taip, kad jungiantis elektronų pora lieka šalia vieno iš atomų ir susidaro jonai. Dalelė su elektronų pora vadinama nukleofiline ir turi neigiamą krūvį (-). Dalelė be elektronų poros vadinama elektrofiline ir turi teigiamą krūvį (+). 44 Cheminių reakcijų tipai

Cheminės reakcijos mechanizmas 45 Reakcijos mechanizmas yra elementarų (paprastų) etapų rinkinys, kuris sudaro tam tikrą reakciją. Reakcijos mechanizmas dažniausiai apima šiuos etapus: reagento aktyvinimas susidarant elektrofilui, nukleofilui ar laisvajam radikalui. Reagentui suaktyvinti paprastai reikalingas katalizatorius. Antrame etape aktyvuotas reagentas sąveikauja su substratu. Tokiu atveju susidaro tarpinės dalelės (tarpinės). Pastarieji apima -kompleksus, -kompleksus (karbokacijas), karbanjonus, naujus laisvuosius radikalus. Paskutiniame etape vyksta tam tikros dalelės pridėjimas arba pašalinimas į (iš) antrojoje stadijoje susidariusį tarpinį produktą, susidarant galutiniam reakcijos produktui. Jei reagentas suaktyvina generuoja nukleofilą, tai yra nukleofilinės reakcijos... Jie pažymėti raide N - (rodyklėje). Tuo atveju, kai reagentas sukuria elektrofilą, reakcijos vyksta elektrofiliškai (E). Tą patį galima pasakyti ir apie laisvųjų radikalų reakcijas (R).

Nukleofilai yra reagentai, turintys neigiamą krūvį, arba atomas, praturtintas elektronų tankiu: 1) anijonai: OH-, CN-, RO-, RS-, Hal- ir kiti anijonai; 2) neutralios molekulės su vienišų elektronų poromis: NH3, NH2R, H2O, ROH ir kt .; 3) molekulės, turinčios perteklinį elektronų tankį (turinčios - ryšius). Elektrofilai yra reagentai, turintys teigiamą krūvį arba atomą, išeikvotą elektronų tankyje: 1) katijonai: Н + (protonas), НSO 3 + (vandenilio sulfonio jonas), NO 2 + (nitronio jonas), NO (nitrozonio jonas) ir kiti katijonai; 2) neutralios molekulės su laisva orbita: AlCl 3, FeBr 3, SnCl 4, BF 4 (Lewiso rūgštys), SO 3; 3) molekulės su išeikvotu elektronų tankiu ant atomo. 46



49

50

51

52


Bioorganinė chemija yra fundamentalus mokslas, tiriantis svarbiausių gyvosios medžiagos komponentų, visų pirma biopolimerų ir mažos molekulinės masės bioreguliatorių, struktūrą ir biologines funkcijas, daugiausia dėmesio skiriant junginių struktūros ir jų biologinio veikimo sąsajų išaiškinimui.
Bioorganinė chemija yra mokslas, esantis chemijos ir biologijos sankirtoje, jis prisideda prie gyvų sistemų funkcionavimo principų atskleidimo. Bioorganinė chemija turi ryškų praktinį dėmesį, kuri yra teorinis pagrindas gauti naujų vertingų junginių medicinos, žemės ūkio, chemijos, maisto ir mikrobiologinėms pramonės šakoms. Bioorganinės chemijos interesų sritis yra neįprastai plati - tai ir medžiagų, izoliuotų nuo gyvosios gamtos, vaidinančių svarbų vaidmenį gyvenime, ir dirbtinai gautų biologinių veikliųjų organinių junginių pasaulis. Bioorganinė chemija apima visų gyvoje ląstelėje esančių medžiagų, dešimčių ir šimtų tūkstančių junginių chemiją.
Tyrimo objektai, tyrimo metodai ir pagrindinės bioorganinės chemijos užduotys
Tyrimo objektai bioorganinė chemija yra baltymai ir peptidai, angliavandeniai, lipidai, mišrūs biopolimerai - glikoproteinai, nukleoproteinai, lipoproteinai, glikolipidai ir kt., alkaloidai, terpenoidai, vitaminai, antibiotikai, hormonai, prostaglandinai, feromonai, toksinai, taip pat sintetiniai biologinių procesų reguliatoriai. : vaistai, pesticidai ir kt.
Pagrindinis tyrimo metodų arsenalas bioorganinės chemijos metodai; fiziniai, fizikocheminiai, matematiniai ir biologiniai metodai naudojami struktūrinėms problemoms spręsti.
Pagrindinės užduotys bioorganinė chemija yra:
- Tiriamų junginių išskyrimas individualioje būsenoje ir gryninimas naudojant kristalizaciją, distiliaciją, įvairių tipų chromatografiją, elektroforezę, ultrafiltraciją, ultracentrifugavimą ir kt. Šiuo atveju dažnai naudojamos specifinės tiriamos medžiagos biologinės funkcijos (pavyzdžiui, antibiotiko grynumas stebimas jo antimikrobiniu aktyvumu, hormonas - jo įtaka tam tikram fiziologiniam procesui ir kt.);
- Nustatyti struktūrą, įskaitant erdvinę struktūrą, remiantis organinės chemijos metodais (hidrolizė, oksidacinis skilimas, skilimas specifiniais fragmentais, pavyzdžiui, metionino liekanomis nustatant peptidų ir baltymų struktūrą, skilimas 1,2-diolio angliavandenių grupėmis ir kt.) Ir fizinis -cheminė chemija naudojant masių spektrometriją, įvairių tipų optinę spektroskopiją (IR, UV, lazerį ir kt.), Rentgeno struktūrinę analizę, branduolinį magnetinį rezonansą, elektronų paramagnetinį rezonansą, optinio sukimosi ir žiedinio dichroizmo dispersiją, greitosios kinetikos metodus ir kt. kartu su skaičiavimais kompiuteryje. Norint greitai išspręsti standartines problemas, susijusias su daugelio biopolimerų struktūros sukūrimu, buvo sukurti ir plačiai naudojami automatiniai įtaisai, kurių principas pagrįstas standartinėmis natūralių ir biologiškai aktyvių junginių reakcijomis ir savybėmis. Tai analizatoriai, leidžiantys nustatyti kiekybinę peptidų aminorūgščių sudėtį, sekvenceriai, skirti patvirtinti ar nustatyti aminorūgščių liekanų seką peptiduose ir nukleotidų sekas nukleorūgštyse ir kt. Fermentų, specialiai skaidančių tiriamus junginius griežtai apibrėžtomis jungtimis, naudojimas yra labai svarbus tiriant sudėtingų biopolimerų struktūrą. Tokie fermentai naudojami tiriant baltymų (tripsino, proteinazių, skaidančių peptidinius ryšius glutamo rūgšties, prolino ir kitų aminorūgščių liekanose), nukleorūgščių ir polinukleotidų (nukleazių, restrikcijos fermentų), angliavandenių turinčių polimerų (glikozidazių, įskaitant specifines galaktozidazes) struktūrą. , gliukuronidazės ir kt.). Siekiant padidinti tyrimų efektyvumą, analizuojami ne tik natūralūs junginiai, bet ir jų dariniai, turintys būdingų specialiai įvestų grupių ir pažymėtų atomų. Tokie dariniai gaunami, pavyzdžiui, auginant augintoją terpėje, kurioje yra pažymėtų aminorūgščių ar kitų radioaktyviųjų pirmtakų, tarp kurių yra tritis, radioaktyvioji anglis arba fosforas. Tyrus sudėtingus baltymus gautų duomenų patikimumas žymiai padidėja, jei šis tyrimas atliekamas kartu su atitinkamų genų struktūros tyrimais.
- Tirtų junginių cheminė sintezė ir cheminė modifikacija, įskaitant visišką sintezę, analogų ir darinių sintezę. Mažos molekulinės masės junginiams priešsintezė vis dar yra svarbus nustatytos struktūros teisingumo kriterijus. Natūralių ir biologiškai aktyvių junginių sintezės metodų kūrimas yra būtinas norint išspręsti kitą svarbią bioorganinės chemijos problemą - išsiaiškinti jų struktūros ir biologinės funkcijos ryšį.
- Biopolimerų ir mažos molekulinės masės bioreguliatorių struktūros ir biologinių funkcijų ryšio išaiškinimas; jų biologinio veikimo cheminių mechanizmų tyrimas. Šis bioorganinės chemijos aspektas įgauna vis daugiau praktinės reikšmės. Sudėtingų biopolimerų (biologiškai aktyvių peptidų, baltymų, polinukleotidų, nukleorūgščių, įskaitant aktyviai veikiančius genus) cheminės ir chemofermentinės sintezės metodų arsenalo tobulinimas kartu su vis tobulėjančia palyginti paprastesnių bioreguliatorių sintezės technika, taip pat selektyvaus biopolimerų skaidymo metodai leidžia vis giliau suprasti biologinio veikimo priklausomybę nuo junginių struktūros. Naudojant labai efektyvią skaičiavimo technologiją galima objektyviai palyginti daugybę skirtingų tyrėjų duomenų ir rasti bendrus modelius. Rasti konkretūs ir bendri modeliai savo ruožtu skatina ir palengvina naujų junginių sintezę, o tai daugeliu atvejų (pavyzdžiui, tiriant smegenų veiklai įtakos turinčius peptidus) leidžia rasti praktiškai svarbius sintetinius junginius, kurių biologinis aktyvumas yra pranašesnis už natūralius jų analogus. Cheminių biologinio veikimo mechanizmų tyrimas atveria galimybę sukurti iš anksto nustatytų savybių biologiškai aktyvius junginius.
- Praktiškai vertingų vaistų gavimas.
- Gautų junginių biologinis tyrimas.
Bioorganinės chemijos formavimas. Istorinė nuoroda
Bioorganinės chemijos atsiradimas pasaulyje įvyko 50-ųjų pabaigoje - 60-ųjų pradžioje, kai pagrindiniai šios srities tyrimų objektai buvo keturios organinių junginių klasės, kurios vaidina pagrindinį vaidmenį ląstelės ir organizmo gyvenime - baltymai, polisacharidai ir lipidai. Puikūs tradicinių natūralių junginių chemijos laimėjimai, tokie kaip L. Pauling atrado α-spiralę kaip vieną iš pagrindinių baltymuose esančios polipeptido grandinės erdvinės struktūros elementų, A. Todd nustatė nukleotidų cheminę struktūrą ir pirmąją dinukleotido sintezę, sukūrė F. Sengerą metodą nustatyti aminorūgščių seką baltymuose. ir insulino struktūros iššifravimas, tokių sudėtingų natūralių junginių kaip rezerpinas, chlorofilas ir vitaminas B12 sintezė R. Woodwardo, pirmojo peptido hormono oksitocino sintezė iš esmės pažymėjo natūralių junginių chemijos virsmą šiuolaikine bioorganine chemija.
Tačiau mūsų šalyje susidomėjimas baltymais ir nukleorūgštimis atsirado daug anksčiau. Pirmieji baltymų ir nukleorūgščių chemijos tyrimai pradėti 1920-ųjų viduryje. tarp Maskvos universiteto sienų ir būtent čia buvo suformuotos pirmosios mokslo mokyklos, sėkmingai dirbančios šiose svarbiausiose gamtos mokslų srityse iki šių dienų. Taigi, 20-ajame dešimtmetyje. N. D. iniciatyva Zelinsky pradėjo sistemingus baltymų chemijos tyrimus, kurių pagrindinis uždavinys buvo išsiaiškinti bendri principai baltymų molekulių struktūra. N. D. Zelinsky sukūrė pirmąją mūsų šalyje baltymų chemijos laboratoriją, kurioje buvo atliktas svarbus darbas dėl aminorūgščių ir peptidų sintezės ir struktūrinės analizės. Nepaprastas vaidmuo kuriant šiuos darbus tenka M.M. Botvinnik ir jos mokiniai, pasiekę įspūdingų rezultatų, tyrinėdami neorganinių pirofosfatazių, pagrindinių fosforo apykaitos ląstelėje fermentų, struktūrą ir veikimo mechanizmą. 40-ųjų pabaigoje, kai pradėjo ryškėti pagrindinis nukleorūgščių vaidmuo genetiniuose procesuose, M.A. Prokofjevas ir Z.A. Šabarova pradėjo nukleorūgščių komponentų ir jų darinių sintezės darbus, taip padėdamas pagrindą mūsų šalies nukleorūgščių chemijai. Buvo atliktos pirmosios nukleozidų, nukleotidų ir oligonukleotidų sintezės, daug prisidėta kuriant buitinius automatinius nukleorūgščių sintezatorius.
60-aisiais. ši kryptis mūsų šalyje vystėsi nuosekliai ir greitai, dažnai lenkdama panašius žingsnius ir tendencijas užsienyje. Plėtojant bioorganinę chemiją, esminiai A.N. Belozerskis, kuris įrodė DNR egzistavimą aukštesniuose augaluose ir sistemingai tyrė cheminę nukleorūgščių sudėtį, klasikiniai V.A. Engelhardtas ir V.A. Belitseris apie fosforilinimo oksidacinį mechanizmą, visame pasaulyje žinomi A.E. Arbuzovas apie fiziologiškai aktyvių fosforo organinių junginių chemiją, taip pat apie pagrindinius I.N. Nazarova ir N.A. Preobraženskis apie įvairių natūralių medžiagų ir jų analogų sintezę bei kitus darbus. Didžiausi nuopelnai kuriant ir plėtojant bioorganinę chemiją SSRS priklauso akademikui M.M. Šemjakinas. Visų pirma jis pradėjo tyrinėti netipinius peptidus - depsipeptidus, kurie vėliau buvo plačiai išplėtoti atsižvelgiant į jų kaip jonoforų funkciją. Šio ir kitų mokslininkų talentas, veržlumas ir energinga veikla prisidėjo prie spartaus sovietinės bioorganinės chemijos tarptautinio prestižo augimo, jos įtvirtinimo aktualiausiose srityse ir organizacinio stiprinimo mūsų šalyje.
60-ųjų pabaigoje - 70-ųjų pradžioje. Sintezuojant biologiškai aktyvius kompleksinės struktūros junginius, fermentai pradėti naudoti kaip katalizatoriai (vadinamoji kombinuota cheminė-fermentinė sintezė). Šį požiūrį G. Korana panaudojo pirmai genų sintezei. Fermentų naudojimas leido atlikti griežtą selektyvų daugelio natūralių junginių transformavimą ir gauti naujus biologiškai aktyvius peptidų, oligosacharidų ir nukleorūgščių darinius su dideliu derlingumu. 70-aisiais. Intensyviausiai išplėtotos bioorganinės chemijos sritys yra oligonukleotidų ir genų sintezė, ląstelių membranų ir polisacharidų tyrimas, baltymų pirminės ir erdvinės struktūros analizė. Buvo tiriamos svarbių fermentų (transaminazės, β-galaktozidazės, nuo DNR priklausomos RNR polimerazės), apsauginių baltymų (γ-globulinų, interferonų), membraninių baltymų (adenozino trifosfatazių, bakteriorodopsino) struktūros. Didelę reikšmę įgijo peptidų - nervų veiklos reguliatorių (vadinamųjų neuropeptidų) - struktūros ir veikimo mechanizmo tyrimai.
Šiuolaikinė buitinė bioorganinė chemija
Šiuo metu buitinė bioorganinė chemija užima pirmaujančias pozicijas pasaulyje daugelyje pagrindinių sričių. Didelė pažanga padaryta tiriant biologiškai aktyvių peptidų ir kompleksinių baltymų, įskaitant hormonus, antibiotikus, neurotoksinus, struktūrą ir funkciją. Gauti svarbūs membraną veikiančių peptidų chemijos rezultatai. Ištirtos unikalaus dispepidų-jonoforų veikimo selektyvumo ir efektyvumo priežastys, išaiškintas veikimo gyvenamosiose sistemose mechanizmas. Gauti sintetiniai norimų savybių jonoforų analogai, kurie efektyvumu daug kartų pranašesni už natūralius mėginius (VT Ivanovas, Yu.A. Ovchinnikovas). Unikalios jonoforų savybės yra naudojamos kuriant jų pagrindu jonų selektyvius jutiklius, kurie plačiai naudojami technologijose. Sėkmės, pasiektos tiriant kitą reguliatorių grupę - neurotoksinus, kurie yra nervinių impulsų perdavimo inhibitoriai, paskatino juos plačiai naudoti kaip įrankius tiriant membraninius receptorius ir kitas specifines ląstelių membranų struktūras (E. V. Grishin). Sukūrus peptidinių hormonų sintezės ir tyrimo darbus, buvo sukurti labai veiksmingi hormonų oksitocino, angiotenzino II ir bradikinino analogai, kurie yra atsakingi už lygiųjų raumenų susitraukimą ir kraujospūdžio reguliavimą. Didžiausia sėkmė buvo visiškas cheminis insulino preparatų, įskaitant žmogaus insuliną, sintezė (N.A. Yudaev, Yu.P.Švačkinas ir kt.). Aptikta ir ištirta daugybė baltyminių antibiotikų, įskaitant gramicidiną S, polimiksiną M, aktinoksantiną (G. F. Gauze, A. S. Khokhlov ir kt.). Aktyviai plėtojamas membraninių baltymų, atliekančių receptorių ir transportavimo funkcijas, struktūros ir funkcijos tyrimas. Gauti fotoreceptorių baltymai rodopsinas ir bakteriorodopsinas ir ištirti jų, kaip nuo šviesos priklausančių jonų siurblių, funkcionavimo fizikiniai ir cheminiai pagrindai (V.P.Skulachev, Yu.A. Ovchinnikov, M.A.Ostrovsky). Ribosomų, pagrindinių baltymų biosintezės ląstelėje sistemų, struktūra ir veikimo mechanizmas buvo plačiai ištirtas (A.S. Spirinas, A. A. Bogdanovas). Dideli tyrimų ciklai siejami su fermentų tyrimais, jų pirminės struktūros ir erdvinės struktūros nustatymu, katalizinių funkcijų (aspartato aminotransferazės, pepsino, chimotripsino, ribonukleazės, fosforo apykaitos fermentų, glikozidazės, cholinesterazės ir kt.) Tyrimais. Sukurti nukleorūgščių ir jų komponentų sintezės ir cheminio modifikavimo metodai (DG Knorre, MN Kolosov, ZA Shabarova), kuriami metodai, kaip sukurti naujos kartos vaistus jų pagrindu virusinėms, onkologinėms ir autoimuninėms ligoms gydyti. Naudojant unikalias nukleorūgščių savybes ir jų pagrindą, diagnostinius preparatus ir biosensorius, daugelio biologiškai aktyvių junginių analizatorius (V.A. Vlasov, Yu.M. Evdokimov ir kt.)
Svarbi pažanga padaryta sintetinėje angliavandenių chemijoje (bakterijų antigenų sintezė ir dirbtinių vakcinų sukūrimas, specifinių virusų sorbcijos ant ląstelių paviršiaus inhibitorių sintezė, specifinių bakterinių toksinų inhibitorių sintezė (N. K. Kočetkovas, A. Ya. Horlinas)). Esminė pažanga padaryta tiriant lipidus, lipoamino rūgštis, lipopeptidus ir lipoproteinus (L. D. Bergelson, N. M. Sissakian). Sukurti daugelio biologiškai aktyvių riebalų rūgščių, lipidų ir fosfolipidų sintezės metodai. Ištirtas lipidų pasiskirstymas transmembranoje įvairių tipų liposomose, bakterijų membranose ir kepenų mikrosomose.
Svarbi bioorganinės chemijos sritis yra įvairių natūralių ir sintetinių medžiagų, galinčių reguliuoti įvairius gyvose ląstelėse vykstančius procesus, tyrimas. Tai yra repelentai, antibiotikai, feromonai, signalinės medžiagos, fermentai, hormonai, vitaminai ir kiti (vadinamieji mažos molekulinės masės reguliatoriai). Sukurti beveik visų žinomų vitaminų, reikšmingos steroidinių hormonų ir antibiotikų dalies sintezės ir gamybos metodai. Buvo sukurti pramoniniai metodai gauti daugelį kofermentų, naudojamų kaip terapiniai agentai (kofermentas Q, piridokso fosfatas, tiamino pirofosfatas ir kt.). Siūlomi nauji stiprūs anabolitai, veikiantys geriau už žinomus užsienio narkotikus (aš, V. Torgovas, SN Ananchenko). Ištirta natūralių ir transformuotų steroidų biogenezė ir veikimo mechanizmai. Reikšminga pažanga padaryta tiriant alkaloidus, steroidų ir triterpeno glikozidus bei kumarinus. Originalūs tyrimai buvo atlikti pesticidų chemijos srityje, todėl buvo išleista daugybė vertingų vaistų (IN Kabachnik, NN Melnikov ir kt.). Aktyviai ieškoma naujų vaistų, reikalingų įvairioms ligoms gydyti. Gauta preparatų, įrodžiusių savo efektyvumą gydant daugybę onkologinių ligų (dopano, sarkolizino, fluorafuro ir kt.)
Prioritetinės bioorganinės chemijos plėtros kryptys ir perspektyvos
Prioritetinės tyrimų sritys bioorganinės chemijos srityje yra šios:
- biologiškai aktyvių junginių struktūrinės ir funkcinės priklausomybės tyrimas;
- naujų biologiškai aktyvių vaistų kūrimas ir sintezė, įskaitant vaistų ir augalų apsaugos produktų kūrimą;
- labai efektyvių biotechnologinių procesų tyrimai;
- gyvame organizme vykstančių procesų molekulinių mechanizmų tyrimas.
Orientuoti fundamentiniai tyrimai bioorganinės chemijos srityje yra skirti svarbiausių biopolimerų ir mažos molekulinės masės bioreguliatorių, įskaitant baltymus, nukleorūgštis, angliavandenius, lipidus, alkaloidus, prostaglandinus ir kitus junginius, struktūrai ir funkcijai tirti. Bioorganinė chemija yra glaudžiai susijusi su praktinėmis medicinos ir žemės ūkio problemomis (vitaminų, hormonų, antibiotikų ir kitų vaistų, augalų augimą stimuliuojančių ir gyvūnų bei vabzdžių elgesio reguliatorių gavimas), chemijos, maisto ir mikrobiologinėmis pramonės šakomis. Mokslinių tyrimų rezultatai yra pagrindas kuriant šiuolaikinių medicinos imunodiagnostikos priemonių, medicininių genetinių tyrimų reagentų ir biocheminės analizės reagentų, onkologijoje, virusologijoje, endokrinologijoje, gastroenterologijoje, taip pat cheminėse medžiagose, gaminančių technologijų mokslinę ir techninę bazę. augalų apsaugos ir jų naudojimo žemės ūkyje technologijos.
Pagrindinių bioorganinės chemijos problemų sprendimas yra svarbus tolesnei biologijos, chemijos ir daugelio technikos mokslų pažangai. Neišaiškinus svarbiausių biopolimerų ir bioreguliatorių struktūros ir savybių, neįmanoma suprasti gyvenimo procesų esmės ir juo labiau rasti būdų, kaip kontroliuoti tokius sudėtingus reiškinius kaip paveldimų bruožų dauginimasis ir perdavimas, normalus ir piktybinis ląstelių augimas, imunitetas, atmintis, nervinių impulsų perdavimas ir daug daugiau. Tuo pačiu metu labai specializuotų biologiškai aktyvių medžiagų ir jose dalyvaujančių procesų tyrimas gali atverti iš esmės naujas galimybes chemijos, chemijos technologijų ir inžinerijos plėtrai. Problemos, kurių sprendimas siejamas su tyrimais bioorganinės chemijos srityje, yra griežtai specifinių labai aktyvių katalizatorių sukūrimas (remiantis fermentų struktūros ir veikimo mechanizmo tyrimu), tiesioginis cheminės energijos pavertimas mechanine energija (remiantis raumenų susitraukimo tyrimu), cheminių medžiagų laikymo principų naudojimas technologijose. informacijos perdavimas biologinėse sistemose, daugiakomponentinių ląstelių sistemų savireguliacijos principai, visų pirma selektyvus biologinių membranų pralaidumas ir daug daugiau. Išvardytos problemos yra toli už pačios bioorganinės chemijos ribų, tačiau tai sukuria pagrindines prielaidas šioms problemoms išsivystyti, suteikiant pagrindinę paramą. taškų už biocheminių tyrimų plėtrą, jau susijusių su molekulinės biologijos sritimi. Sprendžiamų problemų plotis ir svarba, metodų įvairovė ir glaudus ryšys su kitomis mokslo šakomis užtikrina spartų bioorganinės chemijos vystymąsi. Maskvos universiteto biuletenis, 2 serija, chemija. 1999. T. 40. Nr. 5. S. 327-329.
Benderis M., Bergeronas R., Komiyama M. Bioorganinė fermentinės katalizės chemija. Per. iš anglų kalbos M.: Mir, 1987, 352 p.
Yakovishin L.A. Pasirinkti bioorganinės chemijos skyriai. Sevastopolis: „Strizhak-press“, 2006, 196 p.
Nikolajevas A.Ya. Biologinė chemija. Maskva: Medicinos informacijos agentūra, 2001.496 p.